Критерії інфаркту. Перші ознаки інфаркту міокарда
Насамперед, слід зауважити, що інфаркт міокарда заслужено вважається найважчою патологією серця, безпосередньо пов'язаною з руйнуванням (некрозом) серцевих тканин.
Цей екстрений патологічний стан обумовлюється розвитком часткової або повної (абсолютної) недостатності кровопостачання певної частини м'язової оболонки серця (міокарда).
Невідкладний стан щоденно забирає десятки тисяч життів по всьому світу, деяким людям, після перенесеної патології доводиться зіткнутися з інвалідністю, яка присвоюється у зв'язку з обмеженнями працездатності, що виникли. Ускладнює діагностику цього екстреного стану кількість форм та різновидів патології, адже різні видиінфаркту симптоматично можуть проявляти себе дуже по-різному.
Атипові форми інфаркту міокарда, точніше, їх клінічні проявиможуть мати атиповий характер, коли класична симптоматика ураження серця повністю відсутня або значно спотворюється.
Нерідко практикуючі лікарі стикаються з ситуаціями, коли екстрений стан, що описується, може маскуватися під інші патології, ніяк не пов'язані з роботою серця. Як результат при діагностуванні проблеми витрачається величезна кількість дорогоцінного часу, патологія прогресує, а прогнози виживання погіршуються.
Щоб зрозуміти, як може поводитися цей невідкладний стан, пропонуємо розглянути, яким чином, на сьогоднішній день, виглядає загальноприйнята класифікація інфаркту міокарда.
- Як класифікують?
- Щодо місця локалізації
- Патології різних типів
- Діагноз субепікардіальний інфаркт
- Діагноз субендокардіального інфаркту
- Діагноз трансмурального інфаркту
- Діагноз – інтрамуральний інфаркт
- За величиною патологічного вогнища
- Первинна, рецидивна, повторна форми
- Неускладнена чи ускладнена патологія
- Типові та атипові
- Основні періоди
Як класифікують?
Отже, прийнята сьогодні, класифікація інфаркту визначає кілька критеріїв, дозволяють віднести наявну патологію до тієї чи іншої класифікаційної групі.
Основні критерії класифікування полягають у наступному:
За топографічним розташуванням, інфаркт може бути:
- правошлуночковим;
- лівошлуночковим (з некротичним ураженням бічних, передніх задніх стінок міокарда, із залученням у процес міжшлуночкової перегородки).

Відповідно до глибини проникнення некротичного вогнища медики виділяють:
- некротичні ураження міокарда субендокардіального типу (з старанністю вогнища некрозу до внутрішнім частинамм'язової оболонки серця);
- ураження тканин субепікардіального типу (вогнище некрозу прилягає до зовнішнім сторонамміокарда);
- патологія трансмурального типу – це, так званий, наскрізний чи проникаючий некроз, коли м'язова оболонка серця уражається всю її товщину;
- ураження інтрамурального типу (з розташуванням некротичного вогнища у товщі м'язових тканин).

Відповідно до розмірів вогнищ некротичного ураження виділяються:
- Інфаркт міокарда великовогнищевого типу;
- Або ж дрібновогнищева патологія.
Відповідно до кількості повторень бувають:
- первинні напади;
- рецидивні стани, що повторюються протягом перших двох місяців після першого інфаркту;
- повторні напади, що виникають після двох місяців від дня первинного виявлення проблеми.
По розвитку ускладнень некротичне ураження міокарда може бути:

Згідно з клінічною картиною, що розвивається, виділяють:
- типову (класичну) форму нападу, коли симптоматика цілком характерна інфаркту м'язової оболонки серця і легко впізнається;
- різні атипові види, які можуть виявляти себе кардинально по-різному.
Увага! Самостійно розпізнати ту чи іншу форму інфаркту неможливо, часто деякі види патології складно діагностуються навіть в умовах спеціального медичного закладу!
Саме тому, помічаючи незрозумілу вам симптоматику, краще не займатися самолікуванням, не втрачати дорогоцінного часу, а відразу звертатися за кваліфікованою медичною допомогою.
Щодо місця локалізації
Як ми вже помітили, інфаркт міокарда можливо: з ураженням правого/лівого шлуночка, їх бічний, передньої або задньої стінок, а також з некрозом, що стосується міжшлуночкової перегородки.

Лівошлуночкова патологія зустрічається значно частіше, ніж ураження правої сторонисерця.
Приступ, що характеризується ураженням передніх стінок міокарда, прийнято називати переднім інфарктом.
Симптоматика некротичного ураження передніх стінок лівого шлуночка, найчастіше, класична, проте її інтенсивність може залежати від глибини та обширності некротичного вогнища.
Задній інфаркт, що характеризується розташуванням некрозу вогнища на задній стінці лівого шлуночка, також протікає з класичними симптомами. гострим болемза грудиною, страхом смерті, тахікардією та ін.
Приступ некротичного ураження міокарда, що зветься нижній або базальний інфаркт характеризується розташуванням вогнища некрозу на нижній стінці лівого шлуночка.
Крім того, медики можуть окремо виділяти:

Найчастіше, медики все ж таки використовують узагальнені терміни: правошлуночковий або лівошлуночковий інфаркт міокарда (м'язової оболонки серця).
Патологія, що вражає правий шлуночок, виявляється при розвитку специфічної симптоматики: гіпотензії, тріпотінні передсердь, чистоті легеневих полів, порушеннях ритму, що підтверджується даними ЕКГ.
Інфаркт, що вражає структури лівого шлуночка, вдається розпізнати також після проведення електрокардіограми, на якій чудово видно зв'язки ішемічного пошкодження з наявною клінічною картиною.
ЕКГ підтвердженням некрозу структур лівого шлуночка можуть вважатися: елевація сегментів ST, виявлення патологічних зубців Q.
Патології різних типів
Тут хотілося б приділити увагу класифікації патології по глибині проникнення некрозу в стінки міокарда. Відповідно до даної класифікації медики виділяють напади субендокардіального, субепікардіального, трансмурального чи інтрамурального типу.
Діагноз субепікардіальний інфаркт

Термін може мати місце при розташуванні некротичного вогнища безпосередньо у ендокарда (внутрішнього шару оболонки серця) лівого шлуночка, коли поразка має вигляд вузької смужки.
На електрокардіограмі за даної форми інфаркту патологічний зубець Q зазвичай не реєструється.
Діагноз субендокардіального інфаркту
Термінологія обґрунтована, коли після гострого ангінозного стану запису кардіограми реєструють зниження сегмента ST, причому у всіх відведеннях.
Зазвичай також відзначається подальше зменшення зубця R, спостерігається формування «коронарного» зубця Т з позитивним або негативним знаком. Такі зміни в записах кардіограми можуть зберігатись більше тижня.
Діагноз трансмурального інфаркту

Термін доречний при розвитку найтяжчого екстреного стану, що характеризується проникаючим некротичним ураженням усієї товщі стінки міокарда (м'язи серця).
Такий інфаркт може бути або великовогнищевим або великим. Дрібними вогнища за такої патології практично не бувають.
Дана патологія не може обійтися без подальшого рубцювання тканин та розвитку тяжкого постінфарктного кардіосклерозу.
Діагноз – інтрамуральний інфаркт
Цей термін має на увазі розвиток такої патології, при якій відтирання тканин відбувається по всій товщі (на всю глибину) міокарда, але без зачіплення патологічним процесом ендокарда або епікарда.
Характерною ознакою такого виду патології є виявлення на ЕКГ глибинних зубців Т з негативними показниками.
За величиною патологічного вогнища
Відповідно до цієї класифікації медики розрізняють: крупноочаговые, мелкоочаговые чи великі форми інфаркту.

Великовогнищеві варіанти некротичного ураження міокарда характеризуються утворенням великого некротичного вогнища (одного або кількох), тяжким перебігом та яскраво вираженою симптоматикою. Прогнози при такій поразці, як правило, не надто сприятливі.
Дрібноосередкова форма інфаркту, в той же час, не може вважатися менш небезпечною. Це також критичний екстрений стан, при якому осередок некрозу може бути помірним.
Даний варіант патології протікає практично без ускладнень (без набряку легень, аневризм чи розрив серця). Небезпека цієї патології полягає у можливості досить швидко трансформуватися у великовогнищеву або велику форму.
Безсумнівно найбільш небезпечним для пацієнта вважається великий інфаркт, у якому ураженими некрозом виявляються майже всі тканини тієї чи іншої відділу міокарда.
Первинна, рецидивна, повторна форми
Як свідчать назви таких видів некрозу серцевого м'яза, екстрений патологічний стан може бути таким, що виникає первинно, рецидивує або повторюється.

Говорячи про первинну патологію, зауважимо, що інфаркт такого типу частіше виникає після сильного стресу, надмірного фізичного чи емоційного навантаження.
Зв'язується первинна патологія із тривало існуючою ішемією тканин. Коли лікарі говорять про рецидивну форму патології, мається на увазі повторення гострого стану протягом двох місяців після первинного нападу.
Часто рецидивуючий інфаркт може розвиватися за недостатньої ефективності лікування, коли пацієнт не дотримується всіх приписів лікаря.
Повторний інфаркт – це екстрений стан, який виникає після двох місяців з дня першого нападу, коли первинне некротичне вогнище вже зарубцювалося.
Треба сказати, кожен наступний напад завжди протікає важче, ніж попередній, помітно погіршуючи прогнози виживання надалі.
Неускладнена чи ускладнена патологія
Як і будь-яке інше захворювання, інфаркт міокарда може протікати самостійно, а може ускладнюватись іншими недугами. Класична неускладнена патологія закінчується рубцюванням раніше уражених тканин, частковим або, в окремих випадках, повним відновленням функцій.
Серед ускладнень даного екстреного стану найчастіше трапляються такі проблеми:

Після розвитку ускладнень первинного екстреного стану прогнози виживання та відновлення функцій завжди негативні. За даними статистики, загальна смертність від ускладнень інфаркту становить практично тридцять відсотків.
Типові та атипові
З формування клінічної картини(за симптоматикою) медики виділяють класичний (типовий) перебіг інфаркту та його атиповий варіант.
Класичний інфаркт має певну стадійність (конкретні стадії інфаркту міокарда, про які йтиметься нижче) і супроводжується цілком характерною, відомою симптоматикою.
Атипові форми патології можуть бути наступними:

Основні періоди
Як ми вже помітили, аналізований екстрений стан, зазвичай, має суворо певну стадійність. Медики поділяють стан ураження серцевих тканин на наступні періоди або стадії інфаркту міокарда:

На закінчення відзначимо, інфаркт - патологія складна (хоча і досить вивчена), що має безліч форм та підвидів.
Самостійно визначитися із діагнозом буває практично неможливо. Саме тому медики наполягають - якщо ви помічаєте симптоматику, подібну до інфарктної, важливо, якнайшвидше, звернутися до лікарів для первинної діагностики, виявлення проблеми.
Адже саме раніше виявлення патології може врятувати пацієнтові життя!
- У Вас часто виникають неприємні відчуттяу сфері серця (біль, поколювання, стискання)?
- Раптом можете відчути слабкість та втому.
- Постійно відчувається підвищений тиск…
- Про задишку після найменшої фізичної напруги і нема чого говорити…
- І Ви вже давно приймаєте купу ліків, сидите на дієті та стежите за вагою.
Як здійснити розшифровку даних з ЕКГ при ознаках інфаркту міокарда?
Щоб встановити діагноз «інфаркт міокарда», використовують спеціальне обладнання електрокардіограф (ЕКГ). Методика, за якою встановлюється факт цієї недуги, досить проста та інформативна. Зазначимо, що в медицині використовуються портативні варіанти даного обладнання, що дозволяють розпізнавати пошкодження серцевого м'яза пацієнта в домашніх умовах для контролю стану здоров'я своїх близьких навіть без залучення дипломованого фахівця. У лікувальних закладах використовують багатоканальне електрокардіографічне обладнання, яке розшифровує отримані дані.
Особливості кровопостачання міокарда
Насамперед, хочеться відзначити механіку кров'яного потоку. Міокард постачається кров'ю з артерій, які починаються від початкової частини аорти, що розширюється, званої цибулиною. Вони наповнюються кров'ю у фазі діастоли, а в іншій фазі – систолі – потік крові закінчується шляхом прикриття аортальними клапанами, які діють під скороченням самого міокарда.
Від лівої вінцевої (коронарної) артерії відходить 2 гілки, які йдуть загальним стволом до лівого передсердя. Їх називають передньою низхідною та огинаючою гілкою. Дані гілки живлять такі відділи серця:
- лівий шлуночок: задні частини та передньобокові;
- ліве передсердя;
- від правого шлуночка частково передню стінку;
- 2/3 частини від міжшлуночкової перегородки;
- АВ-вузол.
Права коронарна артерія (ПК) бере свій початок звідти, звідки й ліва. Далі вона йде по вінцевій борозні, проходячи її і огинаючи правий шлуночок (ПЖ), переходить на задню серцеву стінку і підживлює задню міжшлуночкову борозну.
Кров, що йде цією артерією, дозволяє функціонувати наступним ділянкам:
- праве передсердя;
- задня стінка ПЗ;
- частина лівого шлуночка;
- 1/3 міжшлуночкової перегородки (МЖП).
Від правої ВА відходять діагональні «магістралі» крові, які живлять частини серця:
- передню стінку ЛШ;
- 2/3 МШП;
- ліве передсердя (ЛП).
У половині випадків від вінцевої артерії відходить ще одна діагональна гілка, а в іншій половині – серединна.
Є кілька різновидів коронарного кровопостачання:
- У 85 відсотках випадків задня стінка постачається від правої КА.
- У 7-8% - від лівої КА.
- Рівномірне постачання кров'ю від правої та від лівої КА.
При грамотному «читанні» кардіограми, отриманої при інфаркті міокарда, потрібно розглянути всі ознаки, розуміти процеси, що проходять у серці, точно їх інтерпретувати. Є два типи ознак інфаркту: прямий та реципрокний.
До прямих ознак відносять електроді, що реєструються. Зворотні ознаки (реципрокні) йдуть як протилежні прямим ознакам, що реєструють некроз зворотної серцевої стінки. При аналізі електрокардіограми хворого важливо знати, що таке патологічний зубець Q і патологічний підйом сегмента ST.
Зубець Q називають патологічним у таких умовах:
- Є у відведеннях V1-V.
- У відведення грудних V4-V6 на 25 відсотків перевищує висоту R.
- У І та ІІ на 15% перевищує R.
- III перевищення від R становить 60%.
- У всіх V-відведеннях сегмент вищий на 1 мм від ізолінії, крім грудного.
- У грудних відведеннях 1-3 сегмент перевищено на 2,5 мм від ізолінії, а в 4-6 відведеннях на висоту понад 1 мм.
Для запобігання розширенню площі некрозу потрібна своєчасна та постійна діагностика інфаркту міокарда.
Інфаркт міокарда на ЕКГ: розшифровка
Щоб розшифрувати дані, отримані кардіографом, потрібно знати певні нюанси. На записаному аркуші паперу чітко спостерігаються сегменти із зубцями та без. Вони позначаються латинськими літерами, які відповідає за зняті дані з одного із відділів серцевого м'яза. Дані зубці є показниками ЕКГ, критеріями інфаркту міокарда.
- Q – показує подразнення шлуночкових тканин;
- R – верхівки серцевого м'яза;
- S – дозволяє аналізувати ступінь подразнення стінок міжшлуночкової перегородки. Вектор S спрямований назад вектор R;
- T – «відпочинок» шлуночків серцевого м'яза;
- ST - час (сегмент) "відпочинку".
Щоб зняти дані з різних ділянок серцевого м'яза використовують, як правило, 12 електродів. Для реєстрації інфаркту значущими є електроди, встановлені на ліву частину грудей (фіксують до відведень V1-V6).
При "читанні" отриманої діаграми лікарі використовують методику обчислення довжини між коливаннями. Отримавши дані, можна зробити аналіз ритму биття серця, причому зубці позначають те, з якою силою серце скорочується. Для визначення порушень слід використовувати наступний алгоритм:
- Проаналізувати дані щодо ритму та скорочення серцевого м'яза.
- Провести розрахунок довжини між коливаннями.
- Вирахувати електричну вісьсерця.
- Вивчити комплекс показань під значення Q, R, S.
- Провести аналіз ST-сегменту.
Увага! Якщо стався напад інфаркту міокарда без підйому сегмента ST, причиною тому могли стати розриви утвореної жирової бляшки в кровоносній судині. Це призводить до активного зсідання крові з утворенням тромбу.
Ознаки інфаркту міокарда на ЕКГ
Інфаркт міокарда має прояви різною мірою складності. Існує 4 типи (стадії) інфаркту міокарда, які можна простежити на кардіограмі пацієнта.
Найгостріша стадія
Перша стадія може тривати до трьох діб, будучи найгострішою у всьому перебігу недуги. У початкові етапи першої стадії інфаркту міокарда формується некроз – пошкоджена ділянка, яка може бути двох типів: трансмуральний та інтрамуральний інфаркт міокарда. ЕКГ у період містить такі зміни у показаннях роботи серця:
- Сегмент ST піднятий, утворює опуклу дугу - елевація.
- Сегмент ST збігається із позитивним зубцем T – монофаза.
- Залежно від тяжкості некрозу зубець R зменшуватиметься у висоті.
А реципрокні зміни, відповідно, полягають у збільшенні зубця R.
Гостра стадія
Після цього йде друга стадія, здатна тривати 2-3 тижні. Відбувається зменшення осередку некрозу. У цей час виявляються ЕКГ-ознаки інфаркту міокарда та ішемії внаслідок загиблих кардіоміоцитів у гострий період інфаркту міокарда. На ЕКГ у гострий період відзначаються такі показання електронних датчиків:
- Сегмент ST наближений до ізолінії в порівнянні з даними, отриманими на першій стадії, але він все ще знаходиться вище за неї.
- Формуються патології QS та QR при транс- та нетрансмуральних ушкодженнях серцевого м'яза відповідно.
- Формується від'ємний симетричний зубець T.
Реципрокні зміни протилежні: зубець T збільшується у висоту, а сегмент ST піднімається до ізолінії.
Підгостра стадія інфаркту міокарда
Тривалість третьої за послідовністю стадії ще більша – до 7-8 тижнів. У цей час хвороба починає стабілізуватись, некроз спостерігається у справжніх розмірах. У цьому періоді показання інфаркту на ЕКГ такі:
- Сегмент ST вирівнюється із ізолінією.
- Патології QR та QS зберігаються.
- Зубець T починає заглиблюватись.
Рубцювання
Останній етап протікання інфаркту міокарда, що починається із 5 тижня. Таку назву етап отримав через те, що на місці некрозу починає утворюватися рубець. Даний рубця ділянка не має електричної та фізіологічної активності. Ознаки рубцювання відображаються на ЕКГ такими ознаками:
- Патологічний зубець Q у наявності. Варто пам'ятати, що при транс- та нетрансмуральних недугах спостерігаються патології комплексів QS та QR відповідно.
- Сегмент ST вирівняний із ізолінією.
- Зубець T є позитивним, зниженим або вирівняним (згладженим).
У цей період патологічні зубці можуть повністю зникнути і по ЕКГ не можна буде виявити інфаркт.
Як розпізнати точне місце некрозу
Щоб виявити локалізацію некрозу (інфаркту міокарда) на ЕКГ необов'язково проводити додаткові обстеження. Кардіограма при інфаркті може забезпечити достатню інформацію, щоб виявити передбачувану область. При цьому кардіограма серця трохи відрізнятиметься.
Ще на показання електрообладнання впливають такі фактори:
- час початку захворювання;
- глибина ураження;
- оборотність некрозу;
- локалізація інфаркту міокарда;
- супутні порушення.
Класифікуючи інфаркт з локалізації, можна виділити такі можливі випадки перебігу хвороби:
- інфаркт передньої стінки;
- задньої стінки;
- перегородковий;
- бічний;
- базальний.
Визначення та класифікація зони ураження допомагає оцінити складність та виявити ускладнення хвороби. Наприклад, якщо поразка торкнулася верхню частину серцевого м'яза, воно не буде поширюватися, оскільки вона ізольована. Поразка правого шлуночка зустрічається дуже рідко і має свої особливості при лікуванні.
Наприклад, передньоперегородковий інфаркт на ЕКГ має такий вигляд:
- Гострокінцеві зубці T у 3-4 відведеннях.
- Q – 1-3.
- Сегмент ST має підйом у 1-3 сегменті.
Класифікація інфаркту міокарда щодо ВООЗ
Щоб класифікувати інфаркт міокарда використовують класифікацію ВООЗ. Відрізняє ці норми те, що застосовуються вони тільки для класифікації великовогнищевих ушкоджень, тому за цими нормами легкі форми перебігу хвороби не розглядаються.
За цією класифікацією виділяються такі типи ушкодження:
- Спонтанний. Відбувається через руйнування бляшки холестерину, ерозії тканин.
- Вторинний. Киснева недостатність, спричинена перекриттям кровоносної судини тромбом або спазмом.
- Раптова коронарна смерть. При цьому інфаркті відбувається повне порушення скорочувальної здатності серця з його зупинкою.
- Черезшкірне коронарне втручання. Причиною стає хірургічне втручання, що призводить до пошкоджень судин або серцевого м'яза
- Тромбоз стенту.
- Ускладнення шунтування аорти.
Використовуючи цю кваліфікацію, можна визначити ступінь некрозу і причини, що його породили. Як правило, застосовується для складних форм інфаркту, тому що легені можна визначити за термінами ураження та локалізації.
Класифікація за терміном
Щоб виявити складність ураження, необхідно правильно встановити терміни перебігу хвороби. Як правило, первинно визначають це з анамнезу пацієнта, який містить картку виклику, та після проведення початкового обстеження. Але вони дозволяють лише надати першу допомогу та виконати процедури до виявлення діагнозу.
Етапи інфаркту за терміном:
- Продромальний. Передінфарктний стан, коли починають виявлятися симптоми. Тривалість може сягати місяця.
- Найгостріший. У цьому періоді протікає хвороба з утворенням некрозу. Тривалість близько 2:00.
- Гострий. Відбувається розвиток некрозу протягом 10 днів, який може протікати з повним омертвінням деяких ділянок.
- Підгострий. До п'ятого тижня з початку розвитку хвороби. У цьому етапі перебігу хвороби некрозні ділянки починають рубцюватися.
- Післяінфарктний період протікає з адаптацією серцевих м'язів до нових умов функціонування та з повним формуванням рубця. Може тривати до півроку.
Після того як пройдено реабілітаційний період, зміни на ЕКГ зникають, залишаються ознаки хронічної ішемії.
Увага! Дана класифікація інфаркту за термінами дозволяє лікарям встановити початок розвитку хвороби та обрати правильне лікуваннядля пацієнта
Для успішного лікування інфаркту міокарда важливим є визначення складності та часу початку інфаркту міокарда. ЕКГ використовують для спостереження активності окремих ділянок серцевого м'яза за допомогою системи електродів.
На відео показано навчальну анімацію з того, як визначити інфаркт міокарда: «ЕКГ під силу кожному»
37593 0
2005 року експерти робочої групиБританського Кардіологічного Товариства запропонували нову класифікацію гострих коронарних синдромів(ОКС):
1. ГКС з нестабільною стенокардією (біохімічні маркери некрозу не визначаються);
2. ГКС з некрозом міокарда (концентрація тропоніну Т нижче 1,0 нг\мл або концентрація тропоніну I (тест «AccuTnI») нижче 0,5 нг\мл;
3. ГКС із клінічними ознаками інфаркту міокарда (ІМ) з концентрацією тропоніну Ti ,0 нг\мл або концентрацією тропоніну I (тест «AccuTnI») >0,5 нг\мл.
Існує кілька класифікацій ІМ залежно від вихідних змін ЕКГ, локалізації вогнища некрозу серцевого м'яза чи залежно від часу розвитку патології.
Залежно від термінів появи та характеру перебігу патології виділяють:
- Первинний ІМ;
- Рецидивний ІМ;
- Повторний ІМ.
Залежно від вихідних змін на ЕКГ виділяють:
- Інфаркт міокарда без підйому сегмента ST;
- ІМ із підйомом сегмента ST без патологічного зубця Q;
- ІМ з підйомом сегмента ST із патологічним зубцем Q.
Залежно від обширності та локалізації вогнища некрозу виділяють:
- Дрібноосередковий ІМ;
- Великовогнищевий ІМ;
- Трансмуральний ІМ;
- Циркулярний (субендокардіальний);
- ІМ передньої стінки лівого шлуночка;
- ІМ бічної стінки лівого шлуночка;
- ІМ задньої стінки лівого шлуночка;
- ІМ нижньої стінки лівого шлуночка (діафрагмальний);
- ІМ правого шлуночка.
Діагностичні критерії ІМ:
- Наявність типових стенокардитичних болів за грудиною («болі ішемічного типу»), які продовжуються понад 30 хвилин;
- Типові зміни ЕКГ;
- Збільшення концентрації в крові маркерів ушкодження міоцитів (Міоглобін; Тропонін - ТнI, ТнТ; КФК - MB фракція; Трансамінази - АСТ/АЛТ; Лактатдегідрогеназа).
Для встановлення діагнозу «достовірний» ІМ необхідна наявність 2 з 3 вище перерахованих критеріїв
Клінічна картина інфаркту міокарда
Класичні клінічні ознакиГІМ були описані J.B. Herrick у 1912 році: стискаючий біль у ділянці грудної клітки з локалізацією за грудиною, що часто поєднується з поширенням у шию, руку або спину (міжлопаткову область) тривалістю більше 30 хвилин, для усунення якої потрібно прийому опіатів. Біль не рідко поєднувався із утрудненим диханням, нудотою, блюванням, переднепритомним станом та відчуттями загрозливої загибелі. Однак ці клінічні ознаки в деяких випадках можуть бути відсутніми або модифікуватися, а відчуття тривоги передувати появі загрудинних болів (продормальні симптоми).
Клінічна картина ІМ різноманітна і за наявності симптомів та характеру скарг виділяють клінічні варіанти початку захворювання.
- Ангінальний варіант- типовий інтенсивний біль за грудиною, що давить, триває більше 30 хвилин і не купується прийомом таблетованих або аерозольних форм органічних нітратів. Біль досить часто іррадіює в ліву половину грудної клітки, нижню щелепу, ліву рукуабо спину, супроводжується почуттям тривоги, страхом смерті, слабкістю, рясним потовиділенням. Даний симптомокомплекс має місце у 75-90% спостережень.
- Астматичний варіант- Ішемічна поразка серця маніфістується задишкою, утрудненим диханням, серцебиттям. Больовий компонент відсутній або мало виражений. Однак, при ретельному опитуванні пацієнта можна виявити, що біль передував розвитку задишки. Частота даного клінічного варіанту ІМ реєструється у 10% серед пацієнтів старшої вікової групи та при повторних ІМ.
- Гастралгічний (черевний) варіант- біль локалізується в областях верхньої половиниживота, мечоподібного відростка, часто іррадіює у міжлопатковий простір, і, як правило, поєднується з диспептичними розладами (гикавка, відрижка, нудота, блювання), симптомами динамічної непрохідності кишечника (здуття живота, ослаблені шуми перестальтаки). Гастралгічний варіант найчастіше зустрічається при нижньому ІМ і вбирається у 5% всіх випадків кардіальної катастрофи.
- Аритмічний варіант- провідною скаргою є почуття «завмирання», перебої у роботі серця, серцебиття, що супроводжуються розвитком різкої слабкості, синкопальних станів чи інших невротичних симптомів, внаслідок погіршення мозкового кровообігу на фоні зниженого артеріального тиску. Біль відсутній чи привертає увагу хворого. Частота аритмічного варіанта коливається не більше 1-5 % випадків.
- Цереброваскулярний варіант- запаморочення, дезорієнтація, непритомність, нудота і блювання центрального генезу, спричинені зниженням перфузії головного мозку. Причиною погіршення мозкового кровообігу є порушення насосної функції серця зі зниженням МО крові на фоні тахіаритмії (параксизм тахіаритмій) або передозування нітратами. Частота розвитку церебровасклярного варіанта ІМ збільшується з віком пацієнтів і коливається від 5 до 10% від загального числа захворювання.
- Малосимптомний варіант- Виявлення ІМ при ЕКГ дослідженніОднак при ретроспективному аналізі анамнезу захворювання в 70-90% випадків пацієнти вказують на попередню невмотивовану слабкість, погіршення настрою, появу дискомфорту в грудній клітціабо почастішання нападів стенокардії, що супроводжуються задишкою, перебоями в серці. Подібний клінічний варіант ІМ найчастіше зустрічається у старших вікових групах із супутнім ЦД 2 типу – від 0,5 до 20%.
Електрокардіографічні зміни при ІМ
Стандартна електрокардіографія (12 відведень) є одним з основних методів, що дозволяють уточнити діагноз ІМ, його локалізацію та широкість ураження серцевого м'яза, наявність ускладнень – характер порушення ритму серцевої діяльності та провідності.
Характерними ознаками ІМ при реєстрації ЕКГ є наявність патологічного зубця Q (ширина – 0,04 сек, глибина перевищує 25% амплітуди зубця R), зниження вольтажу зубця R – зона некрозу; зміщення сегмента ST вище або нижче ізолінії на 2 см (підйом ST сегмента - субепікардіальний шар, зниження ST сегмента - субендокардіальний шар) - зона ішемічного ушкодження; поява гострих, позитивних чи негативних, «коронарних» зубців Т – ішемія (Рис. 1).
Мал. 1.
В даний час, у клінічній практиці, залежно від наявності або відсутності патологічного зубця Q на ЕКГ виділяють «Q-утворюючий» (великовогнищевий або трансмуральний) і «Q-неутворюючий» (субендокардіальний, субепікардіальний, інтрамуральний) інфаркти міокарда. Подібні зміни на ЕКГ відповідають наявності нестабільної атеросклеротичної бляшки та розвитку тромбу на поверхні травмованої бляшки з частковою або повною оклюзією коронарної артерії. (Мал. 2).

Мал. 2.Динаміка нестабільної бляшки з формуванням тромбу та характерних змін на ЕКГ.
Для «Q-утворюючого» ІМ на ЕКГ реєструються характерні зміни:
- Поява патологічних Q-зубців або комплексу QS (некроз серцевого м'яза);
- Зменшення амплітуди зубця R;
- Підйом (елевація) або зниження (депресія) сегментів ST відповідних ділянок (відповідно субепікардіальний або субендокардіальний шари) ішемічного пошкодження;
- Можлива поява блокади лівої ніжки пучка Гіса.
Для «Q-неутворюючого» ІМ характерні такі зміни на ЕКГ:
- Зміщення сегментів ST від ізолінії: елевація – субепікардіальний шар, депресія – субендокардіальний шар;
- Зменшення амплітуди зубця R;
- Двофазність або інверсія зубця Т;
- Відсутність Q-зубця.
Безумовно, велике значення в ЕКГ-діагностиці ІМ є можливість зіставлення з попередньої передінфарктного періоду ЕКГ та добовий моніторинг.
З практичної точки зору найбільш ранніми ознакамирозвитку ІМ є зсув сегмента ST від ізолінії на 2 см і більше, які зазвичай передують появі зубця Q, і можуть реєструватися через 15-20 хвилин від початку больового синдрому.
Для ІМ характерним є динаміка змін ЕКГ залежно від термінів його розвитку та етапів репаративних процесів у зоні некрозу.
Зміщення сегментів ST реєструються на ЕКГ у перші години захворювання, і можуть зберігатися до 3-5 діб, з подальшим поверненням до ізолінії та формуванням глибокого негативного або двофазного зубця Т. При великих ІМ зсув сегмента ST може зберігатися протягом декількох тижнів.
Тривала елевація сегмента ST з QS зубцем («застигла ЕКГ») може відображати епістенокардитичний перикардит трансмурального ІМ, а при одночасному наявності R aVR (симптом Гольдбергера) є ознакою аневризми серця, що формується.
Після 3-4 годин від початку ішемічної атаки на ЕКГ реєструється Q-зубець (некроз міокарда) у відведеннях зі зміщеним сегментом ST. Одночасно у протилежних відведеннях реєструється реципрокне (дискордантне) зниження ST-сегменту, що свідчить про гостроту патологічного процесу.
Зубець Q - стійка ознака некрозу серцевого м'яза або постінфарктного рубцяОднак у деяких випадках він може зменшитися або зникнути (через кілька років) - у випадках компенсаторної гіпертрофії волокон міокарда, що оточують вогнище некрозу або рубця.
Для ІМ характерне формування глибокого, негативного, симетричного Т - зубця («коронарного») на 3-5-ту добу захворювання на ЕКГ відведеннях, що відповідають місцю ішемічного пошкодження міокарда, з паралельним поверненням до ізолінії сегмента ST. Негативний Т - зубець, що сформувався, може зберігатися кілька місяців, проте в подальшому він стає позитивним у більшості пацієнтів, що свідчить про його діагностичну ознаку ішемії, а не пошкодження.
Для топічної діагностики ІМ інформативним є реєстрація ЕКГ у 12 стандартних відведеннях: I, II, III, aVR, aVL, aVF та V 1 -6. Майже завжди до некротичного процесу при ішемії міокарда залучаються одночасно суміжні області лівого шлуночка, тому ЕКГ-зміни, характерні для ІМ, спостерігаються у кількох відведеннях, що відповідають різним областям серця.
Передній ІМ- зміни в I, aVL, V 1-3відведення ЕКГ.
Нижній (діафрагмальний) ІМ- зміни в III, aVFвідведення ЕКГ.
Верхівково-бічний ІМ- зміни в II, aVL, V 4-6відведення ЕКГ.
Передньо-перегородковий ІМ- зміни в I, aVL, V 1-4відведення ЕКГ.
Нижньо-бічний ІМ- зміни в II, III, aVL, aVF, V 5,6відведення ЕКГ.
Передньо-перегородково-верхівковий- зміни в I, aVL, V 1-4відведення ЕКГ.
Задній ІМ- Поява зубця r, Rв V 1-2, зміщення перехідної зони з V 3,4в V 2,3, реципрокне зниження сегмента STв V 1-3 відведеннях.
Певні діагностичні труднощі виникають у 12 стандартних відведеннях ЕКГ при задньобазальному ІМ. Для даної локалізації характерна поява лише реципрокних змін: поява зубців r, R у V 1,2 відведеннях, депресія сегмента ST у відведеннях I, V 1-3 та зниження амплітуди зубця R у відведеннях V 5,6 . (Мал. 3). Додаткову інформацію про локалізації заднього ІМ можна отримати при реєстрації відведень V7-9 (з боку спини), в яких можна виявити патологічні зубці Q і характерну динаміку ST-сегменту та зубця Т. Слід пам'ятати, що і у здорових людейможе реєструватися досить глибокий Q-зубець (до 1/3 амплітуди R-зубця). Патологічним 0-зубцем у відведеннях V 7-9 вважається його тривалість >0,03 сек.

Мал. 3.
Реєстрація додаткових відведень у V 4-6 на два ребра вище (2-3 міжребер'я зліва від грудини) необхідна при підозрі на високий передньо-бічний локалізації ІМ, коли зміни на стандартній ЕКГ виявляються тільки у відведенні aVL.
За характером змін у ЕКГ відведення можна побічно судити про місце ураження коронарних артерій. (Таблиця 1).
Таблиця 1. Область ІМ залежно від локалізації оклюзії коронарних артерій
|
Локалізація ІМ |
Оклюзія коронарної артерії |
Зміни ЕКГ |
|
Передній проксимальний |
ЛКА - вище септальної гілки | |
|
Передній серединний |
ЛКА - між септальною та діагональною гілками | |
|
Передній дистальний |
ЛКА – нижче великої діагональної гілки | |
|
Нижній проксимальний |
Огинаюча ЛКА або проксимальний відділ ПКА |
STV5.6, II, III, aVF |
|
Нижній дистальний |
Нижній відділ ПК | |
|
Задній базальний |
Задня огинаюча ЛКА та нижні відділи ПКА |
Реципрокне зниження STV1-3. r, R в V 1-2 |
|
Циркулярний субендокардіальний |
Поразка дрібних гілок ЛКА та ПКА |
Зниження ST сегмента у всіх відведеннях ЕКГ |
Найбільш важкий тип ІМ виникає при зупинці кровотоку в проксимальному відділі передньої міжшлуночкової артерії до першої відходження септальної гілки. Така локалізація оклюзії та припинення кровопостачання великої зони серцевого м'яза має визначальне значення у зниженні серцевого викиду. При такій локалізації ішемічного ураження міокарда, на ЕКГ реєструються підйоми сегмента ST у всіх прекардіальних відведеннях - V 1-6 , I стандартному відведенні і aVL. (Мал.4). Локалізація оклюзії у проксимальному відділі коронарної артерії супроводжується порушенням кровопостачання провідної системи серця з порушенням проведення збудження: характерний розвиток лівого переднього напівблоку; блокади лівої чи правої ніжок пучка Гіса; можлива поява атріовентрикулярної блокади різного ступеня, аж до повної блокади середньої частини пучка Гіса - блокада Мобітц II (блокада Мобітц I - повна блокадана рівні A-Vз'єднання).

Мал. 4.Критичний стеноз проксимального відділу (до відходження септальної гілки) передньої міжшлуночкової коронарної артерії з формуванням передньо-перегородкового ІМ з поширенням на верхівку та бічну стінку лівого шлуночка.
Припинення кровотоку в проксимальному відділі міжшлуночкової артерії нижче місця відходження першої септальної гілки супроводжується розвитком ІМ у передньо-середньому відділі стінки лівого шлуночка, з реєстрацією підйому сегмента ST у V 3-5 та I стандартному відведенні, без порушень проведення збудження у провідній системі серця. (Мал. 5). Передній ІМ часто супроводжується гіпердинамічний тип гемодинаміки - тахікардія з підвищенням АТ (рефлекторне підвищення симптаїкотонії).

Мал. 5.Критичний стеноз у проксимальному відділі передньої низхідної коронарної артерії з формуванням передньо-перегородкового-верхівкового ІМ
При оклюзії передньої міжшлуночкової артерії нижче місця відходження діагональної гілки формується передньо-нижній ІМ з поширенням на верхівку та бічну стінку лівого шлуночка, що маніфістується на ЕКГ зміщенням сегмента I, aVL і V 4-6 відведеннях. ЇМ даної локалізації має менш важку клінічну картину. До цього типу ІМ можуть бути віднесені варіанти, що мають невелику площу ураження і виникає в результаті оклюзії однієї з діагональних гілок лівої коронарної артерії, що веде до ураження бічних відділів лівого шлуночка. На ЕКГ у цьому варіанті ІМ реєструються зміщеннями ST сегмента у відведеннях II, aVL і V 5,6 .(Рис.6).

Мал. 6. ЕКГ ознакипередньо-бічного ІМ з поширенням на нижню стінку ЛШ
Права коронарна артерія кровопостачає нижньо-задню, бічну стінки правого шлуночків та задньо-перегородкову стінку лівого шлуночка. Оклюзії правої та/або задньої огинаючої лівої коронарних артерій супроводжуються ураженням вище зазначених областей, нерідко з розвитком ІМ правого шлуночка. На ЕКГ реєструється поява r, R зубців V 1-3 з реципрокним зниженням ST сегментів у цих же відведеннях, зі зміщенням перехідної зони від V 3,4 V 1,2 . (Мал. 7). Про ураження міокарда правого шлуночка свідчить наявність патологічного Q-зубця у додаткових відведеннях VR 1-3 (симетричні лівим грудним відведенням). Задній ІМ часто ускладнюється розвитком різного ступеня атріовентриклярної блокади.

Мал. 7.Критичний стеноз правої коронарної артерії у сфері відходження гілки тупого краю, з формуванням задньо-нижнього ІМ: на ЕКГ - QШ, aVF, підйом ST сегмента III, aVF, реципрокне зниження ST сегмента у відведеннях V1, 2, зі зміщенням перехідної зони V2.
Задньо-нижній ІМ зазвичай супроводжується розвитком ваготонії, що проявляється брадикардією та гіпотензією (гіпотонічний тип гемодинаміки), яку можна усунути в введенням 0,5 мл Атропіну.
Таким чином, реєстрація ЕКГ (особливо в динаміці) дозволяє поставити діагноз ІМ, його локалізацію, визначити характер та рівень виникнення порушень провідності, ритму серцевої діяльності, що ускладнюють перебіг патології.
Слід пам'ятати, що наведені вище зміни на ЕКГ можуть мати місце і при інших патологіях: гострий перикардит, міокардити, гостре легеневе серце(Масивна ТЕЛА), синдром ранньої реполяризації, гіпертрофія міокарда лівого шлуночка, ішемічний або геморагічний мозковий інсульт, електролітні та ендокринні порушення тощо. Інфарктоподібні зміни Q-зубця або патологічного комплексу QRS на ЕКГ часто реєструються при синдромах передчасного збудження шлуночків (WPW, CLC), при розшаровуванні аневризми висхідного відділу аорти, хронічних пневмоніях та бронхіальній астмі, важких інтоксикаціях різного генезу.
Ферментна діагностика ІМ
Згідно з рекомендаціями ВООЗ при діагностиці ГІМ, поряд із клінічними ознаками та змінами ЕКГ, велике значення мають дослідження кардіоспецифічних маркерів. В даний час відома достатня кількість маркерів загибелі кардіоміоцитів, що мають різний ступіньспецифічності до м'яза серця, які дозволяють оцінити обсяг, терміни розвитку некрозу та характер перебігу захворювання.
Діагностична цінність лабораторної діагностикиІМ суттєво зростає при безбольових формах та при повторних ІМ, миготливій аритмії, наявності імплантованого артифікаційного водія ритму серця (ЕКС), тобто. у ситуаціях, коли ЕКГ-діагностика ІМ скрутна.
В даний час, у клінічній практиці найбільш часто використовують визначення концентрацій наступних специфічних маркерів ураження кардіоміоцитів: міоглобін (Мг), кардіотропоніни (ТнI, ТнТ), Креатин-фосфокіназа (КФК), Аспартатамінотрансфераза (ACT), лактатде ). (Мал. 8).

Мал. 8.Динаміка кардіоспецифічних ферментів при неускладненому перебігу ІМ.
Специфічними для ураження лише кардіоміоцитів (але не міоцитів) скелетних м'язів) є міоглобін, ізоферменти - КФК-МВ фракція, кардіотропонін - Тні, глікогенфосфорилаза - ГФ-ВВ.
Починаючи з 90-х років XX століття з'явилися технічні можливості для визначення та клінічного використання в діагностиці ІМ двох внутрішньоклітинних структурних білків кардіоміоцитів, що свідчать про загибель міокарда. міоглобін ітропонін.
Найбільш раннім та чутливим до пошкодження кардіоміоцитів є міоглобін. Мг – структурний білок міоциту, при ураженні серцевого м'яза визначається у сироватці крові радіоімунним методом. Міоглобіновий тест має високою чутливістюта специфічністю, що перевищують параметри міокард-специфічних цитозольних ізоінзимів Збільшення концентрації Мг у сироватці крові починається через 1-3 години від початку больового синдрому, досягає максимуму до 6-7 годин захворювання і, при неускладненому перебігу ІМ, повертається до норми до кінця першої доби патологічного процесу.
Другий структурний білок кардіоміоцитів – Тропонін, що бере участь у регуляції функції міоциту – скорочення-розслаблення, входить до складу тропоміозин-тропонінового комплексу, складається з трьох поліпептидів (ТнС, Тні та ТнТ). ТнТ має 3 ізоформи: 2 скелетно-м'язові – ТнТ 2,3 та 1 міокардіальну – ТнТ 1 . Серцевий ТНI локалізується лише у міокарді та виділяється при некрозі кардіоміоцитів. Серцевий тропонін ТнТ також використовується як маркер некрозу міокарда, але його вміст може підвищуватися і підвищення скелетної мускулатури. Значення концентрацій ТнТ і Тні починають перевищувати нормальні рівні через 5-12 годин від початку ішемії, досягають піку до кінця першого дня (через24 години) - ТНІ і до кінця другого дня (48 годин) - ТНТ розвитку ІМ. Нормалізація показників цих кардіоспецифічних маркерів закінчується через 5-10 днів.
Ензимна діагностика інфаркту мітокарда є не тільки методом, що доповнює клінічні ознаки, але й самостійним критерієм при прийнятті рішення про тромболітичну терапію, інвазивну реваскляризацію міокарда в перші години розвитку оклюзії атеротромбозом коронарної артерії при ЕКГ-.
У клінічній практиці при діагностиці ІМ широко використовують визначення концентрації у сироватці крові органоспецифічного цитозольного ензиму креатинфосфокінази – КФК. У людини КФК складається з двох субодиниць (М та В), які утворюють 3 форми ізоферментів: ММ – м'язовий тип, ВВ – мозковий тип, MB – серцевий тип ( КФК заг = S КФК-МВ + КФК-ММ + КФК-ВВ). Активність КФК MB фракції при інфаркті міокарда починає збільшуватися через 6 годин, досягає максимуму через 24 години від початку захворювання та повертається до норми до кінця другої доби розвитку ІМ. Діагностично значущим підвищенням активності КФК MB фракції є півтора-, дворазове перевищення норми прийнятої в даній лабораторії. Традиційно рекомендується визначення активності КФК через кожні 6-8 годин з метою визначення обсягу ураження міокарда (площа побудованої кривої активності ізоферменту) та характеру перебігу захворювання (ускладнене, неускладнене).
Амінотрансферази (аспартатаміно- та аланінамінотрансферази) - універсально поширені внутрішньоклітинні (цитоплазматичні та мітохондріальні) ферменти, визначення активності яких традиційно використовується в клінічній практиці для діагностики ІМ. Їх активність починавши збільшуватися до кінця першої доби захворювання, максимуму досягають до кінця другої доби і нормалізується до кінця третьої доби від початку розвитку ІМ. Специфічним для ураження серцевого м'яза є збільшення відношення ACT до АЛТ у 2,5 рази (індекс Де Рітеса). З активним впровадженням та широким використанням у клінічної практикидіагностики ІМ визначення активності КФК та Тн – органоспецифічних ізоензимів, основним мотивом визначення АСТ\АЛТ залишається дешевизна та доступність цих досліджень.
Інший органоспецифічний для міокарда інзим, що використовується в діагностиці ГІМ та коронарнарних синдромів, - лактатдегідрогеназа (ЛДГ), яка складається з 5 ізоферментів, що містять 2 типи поліпептидних ланцюжків (М та Н). Ізофермент, що переважно міститься в серцевому м'язі, містить 4 ідентичні Н-ланцюжки і його позначають як ЛДГ1, а ізофермент, що містить 4 ідентичні М-ланцюжки, маркується як ЛДГ5. Активність специфічних для міокарда ізоферментів ЛДГ починає збільшуватися з кінця першої доби захворювання, максимум досягає до третьої доби і нормалізується до 5-6 дня розвитку ІМ. Активність ЛДГ слід визначати щодобово протягом трьох діб.
Діагностична цінність вищеописаних маркерів ураження кардіоміоцитів залежить від термінів та частоти їх визначення у динаміці розвитку ГІМ. Паогномонічним для ІМ є підвищення активності ферментів не менше ніж у 1,5-2 рази від рівня норми, з подальшим зниженням до нормальних значень.
Тому одноразове використання міокардіальних маркерів у хворих з підозрою на ГІМ неприйнятне і практично повністю знецінює діагностичну значущість даних методик.
Клініко-лабораторні дослідження
У багатьох хворих, що переносять ІМ, відзначається підвищення температури - субфебрилітет, який поєднується з нейтрофільним лейкоцитозом до 12-14 109/л без паличко-ядерного зсуву, характерного для пневмонії. Нейтрофільний лейкоцитоз при ІМ супроводжується помірною еозинофілією. У міру зменшення лейкоцитозу (на 3-4 добу від початку захворювання) у периферичній крові визначається прискорена ШОЕ (симптом «ножиць»), яка залишається підвищеною протягом 1-2 тижнів.
Для ІМ характерні збільшення рівня фібриногену та позитивна реакціяС-реактивний білок.
При дослідженні коагулограми крові в гострому періоді ІМ реєструється тенденція до гіперкоагуляції з появою продуктів деградації фібриногену (ПДФ) та збільшенням концентрації Д-димеру (один з фрагментів ланцюжка фібрину в згустку крові), що свідчать про спонтанну активацію фібринолітичної системи у відповідь.
Ехокардіографічні дослідження при гострому інфаркті міокарда
Починаючи з 1954 року, коли Едлером і Герцем були зроблені перші повідомлення про використання ультразвукової техніки в діагностиці клапанних поразок та вроджених вад серця, ехокардіографія зазнала значних змін від розгортки руху в часі (М-режим) до дво- та тривимірного ультразвукового зображення анатомічних структур і камери серця в реальному часі.
Двовимірне секторальне сканування ультразвуком дозволяє в динаміці оцінити розміри камер, товщину та рух стінок серця, а також порушення замикальних функцій клапанного апарату та внутрішньосерцевих анатомічних структур. Наявність зон гіпокінезії, акінезії, дискенезії дає уявлення про локалізації та розміри інфаркту міокарда, а динамічний нагляд за скороченням цих зон дає цінну інформацію про розвиток патологічного процесу. Оцінка показників внутрішньосерцевої гемодинаміки (фракція серцевого викиду) дає уявлення про розміри ураження та порушення насосної функції серця.
Одним із перспективних методів діагностики життєздатності міокарда є міокардіальна контрастна ехокардіографія. При внутрішньовенному введенні контрастної речовини (фосфоліпіди або альбумін розмірами від 2,5 до 5 мкм) збільшується ехоконтрастність крові в порожнинах серця та мікросудинному руслі міокарда пропорційно до об'єму кровотоку. Сучасні ультразвукові прилади, оснащені новими технологіями, дозволяють швидко зруйнувати в порожнинах серця мікроструктури контрастної речовини і за швидкістю їх подальшого повторного накопичення та вимивання розрахувати абсолютну величину перфузії міокарда (в мл\г\хв), що дозволяє не тільки виявити зони рубцевого та життєздатного . Цей метод дає можливість оцінити ступінь «оглушеності» міокарда та виявити області гібернуючого серцевого м'яза.
Фармакологічна навантажувальна ехо-кардіографія (стрес-ЕхоКГ) з добутаміном (5-10 мкг/кг\хв) дозволяє виявити «гібернувальний» міокард і ступінь його «оглушеності».
Таким чином, за допомогою ехокардіографії можна неінвазивно в динаміці діагностувати область ураження та ступінь порушення насосної функції серця, на підставі чого оцінювати ефективність лікування, що проводиться, і прогнозувати розвиток хвороби.
Однак цей метод має обмежені можливості у випадках анатомічних особливостей грудної клітини (вузьке міжребер'я, порушення анатомічних взаємин органів середостіння) та емфіземотозної зміни легеневої тканини, що перешкоджають поширенню ультразвукового скануючого променя.
Диференційна діагностика
У ряді випадків, гострий інфаркт міокарда необхідно диференціювати з іншими захворюваннями, так як інтенсивний біль у грудній клітці може бути зумовлений різними патологічними процесами в органах грудної, черевній порожнинахта інших системах людського організму.
1. Захворювання серцево-судинної системи:
- Гіпертрофічна кардіоміопатія;
- Гострий перикардит;
- Гострий міокардит;
- Тромбоемболія легеневої артерії;
- Розшаровуюча аневризму аорти.
2. Захворювання легень та плеври:
- Гостра плевро-пневмонія;
- Спонтанний пневмоторакс.
3. Захворювання стравоходу та ШКТ:
- Езофагіти;
- Дивертикулез стравоходу:
- Грижа стравохідного отвору діафрагми;
- Виразкова хвороба шлунка;
- Гострий холецисто-панкреатит.
4. Захворювання опорно-рухового апарату:
- Остеохондроз шийно-грудного відділу хребта;
- Плечовий плексит;
- Міозит;
- Міжреберна невралгія (перепоясуючий лишай).
Таким чином, основними критеріями диференціальної діагностики інфаркту міокарда є:
А – наявність типового стенокардитичного больового нападу або наявність дискомфорту у грудній клітці;
Б – характерні зміни на ЕКГ;
В – збільшення кардіоспецифічних маркерів некрозу серцевого м'яза. Необхідне динамічне моніторування вище зазначених детермінант для оцінки ефективності лікування та профілактики, що проводиться можливих ускладнень, для регламентування тактики реабілітаційного періодута прогнозу життя пацієнтів, які перенесли ІМ.
Інфаркт міокарда. А.М. Шилов
Нерідко запаморочення є наслідком перенесеного гіпертонічного кризу. Воно супроводжується потемнінням в очах, млявістю, дзвоном у вухах, сонливістю, похитуванням під час ходьби.
Основні причини аномального стану в тому, що організму потрібен час, щоб налаштуватися на нові показники артеріального тиску. Допоможуть подолати хворобливий стан фармакологічні препарати, народні рецепти, корективи в режимі дня та харчування.
Вертиго (запаморочення) після усунення гіпертонічного кризу пов'язане з порушеним, нерівномірним мозковим кровотоком. Часті стрибки тиску негативно впливають на стан стінок судин, відбувається їхнє потовщення, порушення проникності. Під час кризи тканини відчувають гостру нестачу в поживних речовин, що надалі проявляється головними нездужаннями, напівнепритомним станом.
В окремих випадках нудота настає від сильного і різкого перепадутиску. Запаморочення може спостерігатися і в стані спокою, і при рухах (навіть незначних!) голови. Найчастіше вертиго посилюється при закритих очах, швидкій ходьбі, нахилах, присіданнях або різкій зміні положення тіла після тривалого сидіннясну.
Болючий стан також може розвинутися за наявності у хворого на гіпоплазію правої хребетної артерії – аномалії, при якій звужений просвіт артерії. Коливання артеріального тиску призводять до виникнення цефалгії, вертиго, нудоти, блювання.
Недуг може бути спровоковано:
- Надмірно швидкими темпами зниження тиску. Важливо, щоб гіпотензивні медикаменти, що приймаються, зменшували його зі швидкістю не більше 30 одиниць/год.
- Супутні захворювання, у т. ч. цукровий діабет, серцеві та судинні патології, захворювання периферичного відділувестибулярного апарату.
- Побічна реакція на фармацевтичні препарати. Особливо це характерно для людей похилого віку.
- Переляком, тривожним чи депресивним станом хворих.
- Клімактеричним періодом у жінок.
- Ускладненнями різного ступеня після різкого підвищення тиску.
До факторів, що підвищують ризик вертиго після гіпертонічного кризу, належать:

Лікування медикаментозними препаратами
При появі запаморочення після гіпертонічного кризу лікування важливо сфокусувати на причину, що спричинила хворобливий стан. Застосування препаратів має бути своєчасним, але лише після всебічного лікарського обстеження, точно встановленої причини патології, що виникла.
Фахівці відзначають, що частіше кризи та пов'язані з ними запаморочення, властиві людям, які страждають від тяжкої форми гіпертонії, що посилюється атеросклерозом. Для запобігання погіршенню стану можуть застосовуватись (за призначенням медиків!) антигіпертензивні фармацевтичні засобирізних груп, у т. ч.:
- Сечогінні: Гіпотіазид (Hypothiazid), Фуросемід (Furosemiduin). Призначаються як монотерапія, при необхідності комбінуються з іншими препаратами.
- Інгібітори АПФ: Периндоприл (Perindoprilum), Каптоприл (Captopril), Лізіноприл (Lisinopril).
- Спазмолітики: Папаверін (Papaverine), Но-шпа (No-spa).
Дія пластиру спрямована:
- на зняття ознак запаморочення;
- Посилення впливу антигіпертензивних медикаментів;
- Поліпшення живлення мозку;
- Підвищення еластичності судин;
- Звільнення від нервозності, втоми.
Допоможуть м'яко врегулювати підвищений тиск, зняти симптоми запаморочення перевірені народні рецепти:
Допомога у домашніх умовах
Наявність запаморочення після гіпертонічного кризу є яскравим підтвердженням, що лікування важливо продовжувати, навіть якщо тиск нормалізувався. У цей період слід перебувати у спокійній обстановці, при погіршенні стану прийняти лежаче положення (підголів'я має бути піднесеним), забезпечити приплив свіжого повітря, постаратися зафіксувати погляд на якомусь предметі.
При сильному збудженні можна прийняти седативний препарат. Якщо стан погіршується терміново викликати карету швидкої допомоги.
Призначене медиками лікування обов'язково слід провести у повному обсязі, щоб не трапився рецидив. Поганість після кризу – сигнал про наявність в організмі деяких патологічних процесів, які можуть посилитися, «вистрілити» будь-якої миті.
Необхідно пам'ятати, що наслідки ускладненого гіпертонічного кризу є дуже небезпечними. Недуга може супроводжуватися:
- Набряком мозку;
- Енцефалопатією;
- Гострим інфарктом міокарда;
- Інсульт;
- Погіршенням (втратою) слуху та зору;
- Еклампсія;
- Гематурія.
Щоб у подальшому запобігти різкому сплеску тиску, важливо внести корективи в харчування:
Слід регулярно контролювати (краще записувати!) Показники артеріального тиску, проходити лікарські огляди, здавати аналіз крові. Корисно зробити електрокардіограму, УЗД серця.
Профілактика запаморочення неможлива без помірної фізичної активності. Добре підходять ходьба — особливо скандинавська, — заняття йогою, плавання. Намагайтеся максимально захистити себе від стресів та позитивно сприймати життя.
(ІМ) залишається найчастішою причиною викликів бригад швидкої медичної допомоги(СМП). Динаміка кількості викликів у м. Москві щодо ІМ протягом трьох років (табл. 1.) відображає стабільність кількості викликів «швидкої допомоги» з приводу ІМ протягом трьох років та сталість співвідношення ускладнених та неускладнених інфарктів міокарда. Щодо госпіталізацій, то загальна їх кількість практично не змінилася з 1997 до 1999 р. У той же час знизився відсоток госпіталізацій хворих з неускладненим ІМ на 6,6% з 1997 до 1999 року.
Таблиця 1. Структура викликів до хворих на ІМ.
|
Показник |
1997 |
1998 |
1999 |
|
Кількість викликів до хворих на ІМ |
|||
|
Неускладненим |
16255 |
16156 |
16172 |
|
Ускладненим |
7375 |
7383 |
7318 |
|
Усього |
23630 |
23539 |
23490 |
|
% до загальному числухворих на серцево-судинні захворювання |
|||
|
Госпіталізовано хворих |
|||
|
Неускладненим ІМ |
11853 |
12728 |
11855 |
|
Ускладненим ІМ |
3516 |
1593 |
3623 |
|
Усього |
15369 |
16321 |
15478 |
|
% госпіталізованих хворих до кількості викликів |
|||
|
Неускладненим ІМ |
79,9 |
78,8 |
73,3 |
|
Ускладненим ІМ |
47,6 |
48,7 |
49,5 |
|
Усього |
65,0 |
69,3 |
65,9 |
ВИЗНАЧЕННЯ
Інфаркт міокарда - невідкладний клінічний стан, зумовлений некрозом ділянки серцевого м'яза внаслідок порушення кровопостачання.
ОСНОВНІ ПРИЧИНИ ВИНИКНЕННЯ ТА ПАТОГЕНЕЗ
Розвивається в рамках ішемічної хворобисерця, є результатом коронарного. Безпосередньою причиною інфаркту міокарда найчастіше є оклюзія або субтотальний стеноз коронарної артерії, що майже завжди розвивається внаслідок розриву або розщеплення атеросклеротичної бляшки з утворенням тромбу, підвищеною агрегацією тромбоцитів та сегментарним спазмом поблизу бляшки.
КЛАСИФІКАЦІЯ
З точки зору визначення обсягу необхідної лікарської терапії та оцінки прогнозу становлять інтерес три класифікації.
А. По глибині поразки (На основі даних електрокардіографічного дослідження):
1. Трансмуральний та великовогнищевий («Q-інфаркт») - з підйомом сегмента ST в
Перший годинник захворювання і формуванням зубця Q в подальшому.
2. Дрібноосередковий («не Q-інфаркт») - не супроводжується формуванням зубця Q, а
Т, що проявляється негативними зубцями Т
Б. За клінічним перебігом:
1. Неускладнений інфаркт міокарда.
2. Ускладнений інфаркт міокарда (див. нижче).
В. По локалізації:
1. Інфаркт лівого шлуночка (передній, задній або нижній, перегородковий)
2. Інфаркт правого желудочка.
КЛІНІЧНА КАРТИНА
За симптоматикою найгострішої фази інфаркту міокарда виділяють такі клінічні варіанти:
|
Больовий (status anginosus) |
- типовий клінічний перебіг, основним проявом при якому служить ангінозна біль, що не залежить від пози та положення тіла, від рухів та дихання, стійка до нітратів; біль має давить, душить, пекучий або роздираючий характер з локалізацією за грудиною, у всій передній грудній стінці з можливою іррадіацією в плечі, шию, руки, спину, епігастальну ділянку; характерні поєднання з гіпергідрозом, різкою загальною слабкістю, блідістю шкірних покривів, збудженням, руховим занепокоєнням. |
|
Абдомінальний (status gastralgicus) |
- проявляється поєднанням епігастральних болів з диспептичними явищами - нудотою, яка не приносить полегшення блюванням, гикавкою, відрижкою, різким здуттям живота; можливі ірадіація болю в спину, напруга черевної стінки та болючість при пальпації в епігастрії. |
|
Атиповий больовий |
- при якому больовий синдром має атиповий характер щодо локалізації (наприклад, тільки в зонах іррадіації - горлі та нижній щелепі, плечах, руках і т.д.) та/або за характером. |
|
Астматичний (status astmaticus) |
- єдиною ознакою при якому є напад задишки, що є проявом гострої серцевої застійної недостатності (серцева астма або набряк легень). |
|
Аритмічний |
- при якому порушення ритму є єдиним клінічним проявом або переважають у клінічній картині. |
|
Цереброваскулярний |
- у клінічній картині якого переважають ознаки порушення мозкового кровообігу (частіше – динамічного): непритомність, запаморочення, нудота, блювання; можлива осередкова неврологічна симптоматика. |
|
Малосимптомний (безсимптомний) |
- найбільш складний для розпізнавання варіант, що часто діагностується ретроспективно за даними ЕКГ. |
ДІАГНОСТИЧНІ КРИТЕРІЇ
на догоспітальному етапінадання медичної допомоги діагноз гострого інфаркту міокарда ставиться на підставі відповідних:
а) клінічної картини
б) змін електрокардіограми.
А. Клінічні критерії.
При больовому варіанті інфаркту іагностичним значенням мають:
- інтенсивність (у випадках, коли аналогічні болі виникали раніше, при інфаркті вони бувають надзвичайно інтенсивними),
- тривалість (незвичайно тривалий напад, що зберігається понад 15-20 хвилин),
- поведінка хворого (збудження, руховий неспокій),
- неефективність сублінгвального прийому нітратів
Таблиця 2.
Перелік питань, обов'язкових під час аналізу больового синдрому у разі підозри на гострий інфаркт міокарда
|
Питання |
Примітка |
|
Коли розпочався напад? |
Бажано визначити якнайточніше. |
|
Скільки часу триває напад? |
Менш 15, 15-20 або більше 20 хв. |
|
Чи були спроби усунути напад нітрогліцерином? |
Чи був хоча б короткочасний ефект? |
|
Чи залежить біль від пози, положення тіла, рухів та дихання? |
При коронарогенному нападі залежить. |
|
Чи були аналогічні напади у минулому? |
Аналогічні напади, які не завершилися інфарктом, потребують диференціальної діагностики з нестабільною стенокардією та не кардіальними причинами. |
|
Чи виникали напади (болі чи ядухи) при фізичного навантаження(ходьбі), чи змушували вони зупинятися, скільки вони тривали (у хвилинах), як реагували на нітрогліцерин? |
Наявність стенокардії напруги робить можливим припущення про гострий інфаркт міокарда. |
|
Чи нагадує справжній напад відчуття, що виникали при фізичному навантаженні по локалізації чи характеру болю? |
За інтенсивністю та супроводжуючими симптомами напад при інфаркті міокарда зазвичай важчий, ніж при стенокардії напруги. |
За будь-якого варіанта допоміжне діагностичне значеннямають:
Гіпергідроз,
Різка загальна слабкість,
Блідість шкірних покривів,
Ознаки гострої серцевої недостатності.
Відсутність типової клінічної картини не може бути доказом відсутності інфаркту міокарда.
Б. Електрокардіографічні критерії - Зміни, що служать ознаками:
|
Пошкодження |
- дугоподібний підйом сегмента ST опуклістю вгору, що зливається з позитивним зубець T або переходить у негативний зубець T (можлива дугоподібна депресія сегмента ST опуклістю вниз); |
|
Великовогнищевого або Трансмуральний інфаркт |
- поява патологічного зубця Q та зменшення амплітуди зубця R або зникнення зубця R та формування QS; |
|
Дрібноосередкового інфаркту |
- поява негативного симетричного зубця T; |
|
Примітки: 1. Непрямою ознакою інфаркту міокарда, що не дозволяє визначити фазу і глибину процесу, є гостра блокада ніжок пучка Гіса (за наявності відповідної клініки). 2. Найбільшу достовірність мають електрокардіографічні дані в динаміці, тому електрокардіограми за будь-якої можливості повинні порівнюватися з попередніми. |
|
При інфаркті передньої стінки подібні зміни виявляються у I та II стандартних відведеннях, посиленому відведенні від лівої руки (aVL) та відповідних грудних відведеннях (V1, 2, 3, 4, 5, 6). При високому бічному інфаркті міокарда зміни можуть реєструватися лише у відведенні aVL і для підтвердження діагнозу необхідно зняти високі грудні відведення. При інфаркті задньої стінки (нижньому, діафрагмальному) ці зміни виявляються у II, III стандартному та посиленому відведенні від правої ноги (aVF). При інфаркті міокарда високих відділів задньої стінки лівого шлуночка (задно-базальному) зміни у стандартних відведеннях не реєструється, діагноз ставиться на підставі реципрокних змін – високих зубців R та Т у відведеннях V 1 -V 2 (таблиця 3).
Мал. 1. Найгостріша фаза трансмурального переднього інфаркту міокарда.
Таблиця 3. Локалізація інфаркту міокарда за даними ЕКГ
|
Тип інфаркту з локалізації |
Стандартні відведення |
Грудні відведення |
|||||||||
|
III |
|||||||||||
|
Перегородковий |
|||||||||||
|
Пердно-перегородковий |
|||||||||||
|
Передній |
|||||||||||
|
Розповсюджений передній |
|||||||||||
|
Передньо-бічний |
|||||||||||
|
Бічний |
|||||||||||
|
Високий боковий |
|||||||||||
|
Задньо-боковий |
|||||||||||
|
Задньо-діафрагмальний |
|||||||||||
|
Задньо-базальний |
|||||||||||
ЛІКУВАННЯ ІНФАРКТУ МІОКАРДУ
Невідкладна терапія має кілька взаємопов'язаних цілей:
1. Купірування больового синдрому.
2. Відновлення коронарного кровотоку.
3. Зменшення роботи серця та потреби міокарда в кисні.
4. Обмеження розмірів інфаркту міокарда.
5. Лікування та профілактика ускладнень інфаркту міокарда.
Лікарські засоби, що застосовуються для цього, представлені в таблиці 3.
Таблиця 3.
Основні напрямки терапії та лікарські засоби, що застосовуються у найгострішій стадії неускладненого інфаркту міокарда
|
Напрями терапії |
||
|
Морфін внутрішньовенно дрібно |
Адекватне знеболювання, зниження перед- та постнавантаження, психомоторного збудження, потреби міокарда в кисні |
2-5 мг внутрішньовенно кожні 5-15 хвилин до повного усунення больового синдрому або до появи побічних ефектів |
|
Стрептокіназа (стрептаза) |
Відновлення коронарного кровотоку (тромболізис), усунення больового синдрому, обмеження розмірів інфаркту міокарда, зниження летальності |
1,5 млн. МО внутрішньовенно за 60 хвилин |
|
Гепарин внутрішньовенно струминно (якщо не проводиться тромболізис) |
Попередження або обмеження коронарного тромбозу, профілактика тромбоемболічних ускладнень, зниження летальності |
10000-15000 МО внутрішньовенно струминно |
|
Нітрогліцерин або ізосорбіду динітрат внутрішньовенно краплинно |
Купірування больового синдрому, зменшення розмірів інфаркту міокарда та летальності |
10 мкг/хв. зі збільшенням швидкості на 20 мкг/хв кожні 5 хвилин під контролем ЧСС та АТ |
|
Бета-адреноблокатори: пропранолол (обзидан) |
Зниження потреби міокарда в кисні, купірування больового синдрому, зменшення розмірів некрозу, профілактика фібриляції шлуночків та розриву лівого шлуночка, повторних інфарктів міокарда, зниження летальності |
1 мг/хв кожні 3-5 хвилин до загальної дози 10 мг |
|
Ацетилсалицилова кислота (аспірин) |
Купірування та профілактика процесів, пов'язаних з агрегацією тромбоцитів; при ранньому(!) призначенні знижує летальність |
160-325 мг розжувати; |
|
Магнію сульфат (кормагнезин) |
Зниження потреби міокарда в кисні, усунення больового синдрому, зменшення розмірів некрозу, профілактика порушень серцевого ритму, серцевої недостатності, зниження летальності |
1000 мг магнію (50 мл 10%, 25 мл 20% або 20 мл 25% розчину) внутрішньовенно протягом 30 хвилин. |
АЛГОРИТМ НАДАННЯ МЕДИЧНОЇ ДОПОМОГИ ХВОРИМ ГОСТРИМ ІНФАРКТОМ МІОКАРДУ НА ДОГОСПІТАЛЬНОМУ ЕТАПІ
А. Неускладнений інфаркт міокарда
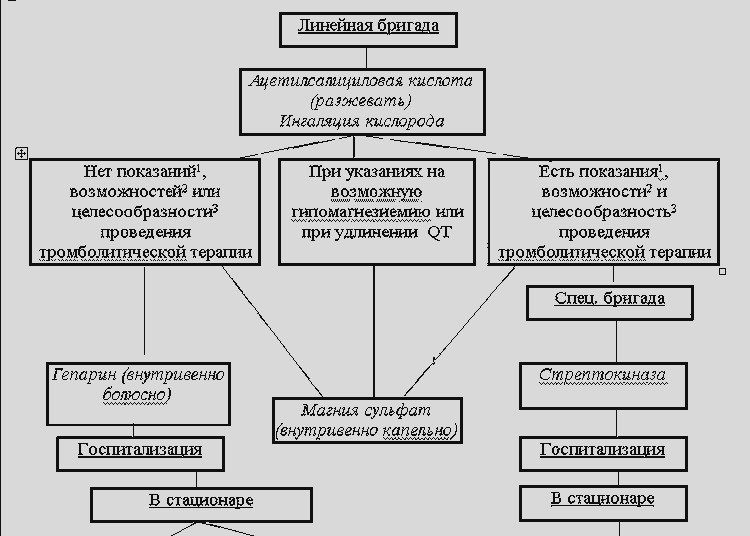

Б. Неускладнений інфаркт міокарда абоінфаркт міокарда, ускладнений наполегливим больовим синдромом

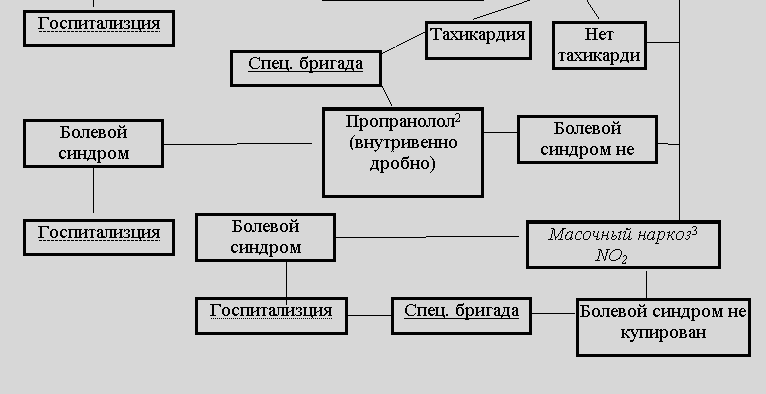
В. Ускладнений інфаркт міокарда

1. Купірування больового нападу
при гострому інфаркті міокарда - одне з найважливіших завдань, оскільки біль через активацію симпатоадреналової системи викликає підвищення судинного опору, частоти та сили серцевих скорочень, тобто збільшує гемодинамічний навантаження на серце, підвищує потребу міокарда в кисні та посилює ішемію.
Якщо попередній сублінгвальний прийом нітрогліцерину (повторно по 0,5 мг у таблетках або 0,4 мг в аерозолі) біль не купірував, починається терапія наркотичними анальгетиками, які мають крім аналгетичної та седативної дії впливом на гемодинаміку: внаслідок вазодилатирующих властивостей вони забезпечують гемодинамічну зменшуючи насамперед переднавантаження. На догоспітальному етапі препаратом вибору для усунення больового синдрому при інфаркті міокарда є морфін, що володіє не тільки необхідними ефектами, але і достатньою для транспортування тривалістю дії. Препарат вводиться внутрішньовенно дробово: 1 мл 1% розчину розводять фізіологічним розчином натрію хлориду до 20 мл (1 мл отриманого розчину містить 0,5 мг активної речовини) і вводять 2-5 мг кожні 5-15 хвилин до повного усунення больового синдрому або до появи побічних ефектів (гіпотензії, пригнічення дихання, блювання). Сумарна доза не повинна перевищувати 10-15 мг (1-1,5 мл 1% розчину) морфіну (на догоспітальному етапі не допускається перевищення дози 20 мг).
При невираженому больовому синдромі, пацієнтам похилого віку та ослабленим хворим наркотичні анальгетики можуть вводитися підшкірно або внутрішньом'язово. Не рекомендується вводити підшкірно більше 60 мг морфіну протягом 12 годин.
Для профілактики та усунення таких побічних ефектів наркотичних анальгетиків як нудота та блювання рекомендують внутрішньовенне введення 10-20 мг метоклопраміду (, реглану). При вираженій брадикардії з гіпотонією або без неї показано використання атропіну у дозі 0,5 мг (0,5 мл 0,1 % розчину) внутрішньовенно; А боротьба зі зниженням артеріального тиску проводиться за загальним принципом корекції гіпотензії при інфаркті міокарда.
Недостатня ефективність знеболювання наркотичними анальгетиками є показанням до внутрішньовенної інфузії нітратів. При низькій ефективності нітратів у поєднанні з тахікардією додатковий знеболюючий ефект може бути отриманий запровадженням бета-адреноблокаторів. Біль може бути усунутий в результаті ефективного тромболізису.
Завзяті інтенсивні ангінозні болі є показанням до застосування масочного наркозу закисом азоту (що володіє седативною та аналгезуючою дією) у суміші з киснем. Починають з інгаляції кисню протягом 1-3 хвилин, потім використовується закис азоту (20%) з киснем (80%) з підвищенням концентрації закису азоту до 80%; після засипання хворого переходять на підтримуючу концентрацію газів - 50´ 50%. Позитивний момент – закис азоту не впливає на функцію лівого шлуночка. Виникнення побічних ефектів - нудоти, блювання, збудження чи сплутаності свідомості - є показанням зменшення концентрації закису азоту чи скасування інгаляції. При виході з наркозу інгалюють чистий кисень протягом 10 хвилин попередження артеріальної гіпоксемії.
Для вирішення питання щодо можливості використання наркотичних аналгетиків слід уточнити ряд моментів:
- переконатися, що типовий чи атиповий больовий синдром не є проявом “гострого живота”, та зміни ЕКГ є специфічним проявом інфаркту міокарда, а не неспецифічною реакцією на катастрофу в черевній порожнині;
- з'ясувати, чи є в анамнезі хронічні захворювання системи дихання, зокрема бронхіальна астма;
- уточнити, коли останнє загострення бронхообструктивного синдрому;
- встановити, чи є нині ознаки дихальної недостатності, які, який ступінь її виразності;
- з'ясувати, чи є у хворого в анамнезі судомний синдромколи був останній напад.
2. Відновлення коронарного кровотоку в найгострішій фазі інфаркту міокарда,
достовірно покращує прогноз, за відсутності протипоказань здійснюється шляхом системного тромболізису.
а). Показаннями до проведення тромболізису служать наявність підйому сегмента ST більш ніж на 1 mm принаймні у двох стандартних відведеннях ЕКГ і більш ніж на 2 mm у двох суміжних грудних відведеннях або гостра повна блокада лівої ніжки пучка Гіса при терміні, що пройшов з початку захворювання, більше 30 хвилин, але не більше 12 годин. Застосування тромболітичних засобів можливе і пізніше у випадках коли зберігаються підйом сегмента ST, продовжується біль та/або спостерігається нестабільна гемодинаміка.
На відміну від внутрішньокоронарного системний тромболізис (здійснюється внутрішньовенним введенням тромболітичних засобів) не потребує якихось складних маніпуляцій та спеціального обладнання. При цьому він досить ефективний, якщо розпочато у перші години розвитку інфаркту міокарда (оптимально – на догоспітальному етапі), оскільки скорочення летальності безпосередньо залежить від термінів його початку.
За відсутності протипоказань вирішення питання про проведення тромболізису ґрунтується на аналізі фактора часу: якщо транспортування у відповідний стаціонар може бути тривалішим, ніж термін до початку цієї терапії спеціалізованою бригадою “швидкої допомоги” (при передбачуваному часі транспортування більше 30 хвилин або при відстроченні внутрішньолікарняного проведення (за 60 хвилин), введення тромполітичних засобів повинно здійснюватися на догоспітальному етапі надання медичної допомоги. Інакше вона має бути відкладена до госпітального етапу.
Найчастіше використовується стрептокіназа. Методика внутрішньовенного введення стрептокінази: введення стрептокінази проводиться лише через периферичні вени, спроби катетеризації центральних вен неприпустимі; перед інфузією можливе внутрішньовенне введення 5-6 мл 25% магнію сульфату, або 10 мл кормагнезину-200 внутрішньовенно струминно, повільно (за 5 хв); "навантажувальна" доза аспірину (250-300 мг - розжувати) дається завжди, за винятком випадків, коли аспірин протипоказаний (алергічні та ); 1500000 Од стрептокінази розводиться в 100 мл ізотонічного розчину хлориду натрію і вводиться внутрішньовенно за 30 хв.
Одночасне призначення гепарину при використанні стрептокінази не потрібно - припускають, що стрептокіназа сама має антикоагуляційні та антиагрегаційні властивості. Показано, що внутрішньовенне введення гепарину не знижує летальність та частоту рецидивів інфаркту міокарда, а ефективність його підшкірного введення є сумнівною. Якщо гепарин з якихось причин було введено раніше, це не є перешкодою для проведення тромболізису. Рекомендується призначення гепарину через 4 години після припинення інфузії стрептокінази. Рекомендоване використання гідрокортизону для профілактики анафілаксії визнано не тільки малоефективним, але і небезпечним в найгострішій стадії інфаркту міокарда (глюкокортикоїди збільшують ризик розриву міокарда).
Основні ускладнення тромболізису
1). Кровотечі (в т.ч. найбільш грізні – внутрішньочерепні) – розвиваються внаслідок пригнічення процесів згортання крові та лізису кров'яних згустків. Ризик розвитку інсульту при системному тромболізі становить 0,5-1,5% випадків, зазвичай інсульт розвивається в першу добу після проведення тромболізису. Для зупинки незначної кровотечі (з місця пункції, з рота, носа) достатньо здавлення ділянки, що кровоточить. При більш значних кровотечах (шлунково-кишковій, внутрішньочерепній) необхідна внутрішньовенна інфузія амінокапронової кислоти - 100 мл 5% розчину вводять протягом 30 хв і далі 1 г/годину до зупинки кровотечі, або транексамової кислоти по 1-1, рази на добу внутрішньовенно крапельно; також ефективно переливання свіжозамороженої плазми. Слід пам'ятати про те, що при використанні антифібринолітичних засобів зростає ризик реоклюзії коронарної артерії та реінфаркту, тому використовувати їх необхідно лише при загрозливих для життя кровотечах.
2). Аритмії, що виникають після відновлення коронарного кровообігу (реперфузійні). Не вимагають інтенсивної терапії повільний вузловий або шлуночковий ритм (при частоті серцевих скорочень менше 120 хв і стабільній гемодинаміці); надшлуночкова та шлуночкова екстрасистолія (у тому числі аллоритмована); атріовентрикулярна блокада I і II (типу Мобіц I) ступеня. Вимагають невідкладної терапії фібриляція шлуночків (необхідна дефібриляція, комплекс стандартних реанімаційних заходів); двонаправлена веретеноподібна шлуночкова тахікардія типу «пірует» (показано дефібриляцію, введення сульфату магнію внутрішньовенно струминно); інші різновиди шлуночкової тахікардії (використовують введення лідокаїну або проводять кардіоверсію); стійка суправентрикулярна тахікардія (купується внутрішньовенним струменевим введенням верапамілу або новокаїнаміду); атріовентрикулярна блокада II (типу Мобітц II) та III ступеня, синоатріальна блокада (внутрішньовенно струминно вводять атропін у дозі до 2,5 мг, при необхідності проводять екстрену електрокардіостимуляцію).
3). Алергічні реакції. Висипання, свербіж, періорбітальний набряк зустрічаються в 4,4% випадків, тяжкі реакції (, анафілактичний шок) - в 1,7% випадків. При підозрі на розвиток анафілактоїдної реакції необхідно негайно зупинити інфузію стрептокінази та ввести внутрішньовенно болюсом 150 мг преднізолону. При вираженому пригніченні гемодинаміки та появі ознак анафілактичного шоку внутрішньовенно вводять 1 мл 1% розчину адреналіну, продовжуючи введення стероїдних гормонів внутрішньовенно краплинно. При пропасниці призначають аспірин або парацетамол.
4). Рецидивування больового синдрому після проведення тромболізису усувається внутрішньовенним дробовим введенням наркотичних анальгетиків. При наростанні ішемічних змін на ЕКГ показано внутрішньовенне краплинне введення нітрогліцерину або якщо інфузія вже налагоджена, - збільшення швидкості його введення.
5). При артеріальній гіпотонії в більшості випадків досить тимчасово припинити інфузію тромболітика і підняти ноги пацієнта; при необхідності рівень АТ коригується введенням рідини, вазопресорів (допаміну або норадреналіну внутрішньовенно крапельно до стабілізації АД систоли на рівні 90-100 мм рт.ст.).

Мал. 2. Реперфузійна аритмія при трансмуральному задньому інфаркті міокарда: епізод вузлового ритму із самостійним відновленням синусового ритму.
Клінічні ознаки відновлення коронарного кровотоку:
- припинення ангінозних нападів через 30-60 хв після введення тромболітика,
- стабілізація гемодинаміки,
- зникнення ознак лівошлуночкової недостатності,
- швидка (протягом кількох годин) динаміку ЕКГ з наближенням сегмента ST до ізолінії та формуванням патологічного зубця Q, негативного зубцяТ (можливе раптове збільшення ступеня підйому сегмента ST з подальшим його швидким зниженням),
- поява реперфузіооних аритмій (прискореного ідіовентрикулярного ритму, шлуночкової екстрасистолії та ін.),
- швидка динаміку МВ-КФК (різке підвищення її активності на 20-40%).
Для вирішення питання щодо можливості використання тромболитичних засобів слід уточнити низку моментів:
- переконатися у відсутності протягом попередніх 10 днів гострих внутрішніх кровотеч - шлунково-кишкової, легеневої, маткової за винятком менструального, гематурії та ін. (звернути увагу на їх наявність в анамнезі) або хірургічних втручань та травм із пошкодженням внутрішніх органів;
- виключити наявність протягом попередніх 2 місяців гостре порушення мозкового кровообігу, операції чи травми головного чи спинного мозку (звернути увагу на їх наявність в анамнезі);
- виключити підозру на гострий панкреатит, що розшаровує аневризму аорти, а також на аневризму церебральної артерії, пухлину головного мозку або метастазуючі злоякісні пухлини;
- встановити відсутність фізикальних ознак або анамнестичних вказівок на патологію системи згортання крові - геморагічний діатез, тромбоцитопенія (звернути увагу на гоморагічну діабетичну ретинопатію);
- переконатися, що хворий не отримує непрямих антикоагулянтів;
- уточнити, чи не було алергічних реакцій на відповідні тромболітичні препарати, а щодо стрептокінази, чи не було попереднього введення в термін від 5 днів до 2 років (у цей період у зв'язку з високим титром антитіл введення стрептокінази неприпустимо);
- у разі проведених успішних реанімаційних заходів переконатися, що вони не були травматичними та тривалими (за відсутності ознак постреанімаційних травм – переломів ребер та пошкодження внутрішніх органів звернути увагу на тривалість, що перевищувала 10 хвилин);
- домогтися стабілізації підвищеного артеріального тиску лише на рівні менше 200/120 мм рт. ст. (Звернути увагу на рівень, що перевищує 180/110 мм рт. ст.)
- звернути увагу на інші стани, небезпечні розвитком геморагічних ускладнень та службовці відносними протипоказаннями до проведення системного тромболізису: тяжкі захворювання печінки або нирок; підозра на хронічну аневризму серця, перикардит, інфекційний міокардит, наявність тромбу у серцевих порожнинах; тромбофлебіт та флеботромбоз; варикозне розширеннявен стравоходу, виразкова хвороба у стадії загострення; вагітність;
- мати на увазі, що ряд факторів, які не є відносними або абсолютними протипоказаннями до проведення системного тромболізису, можуть підвищувати його ризик: вік понад 65 років, маса тіла менше 70 кг, жіноча стать, артеріальна гіпертензія.
Системний тромболізис можливий у літньому та старечому віці, а також на тлі артеріальної гіпотензії (систолічний АТ менше 100 мм рт. ст.) та кардіогенного шоку.
У сумнівних випадках рішення про проведення тромболітичної терапії має бути відстроченим до стаціонарного етапу лікування. Відстрочка показана при атиповому розвитку захворювання, неспецифічних змінах ЕКГ, давно існуючій блокаді ніжки пучка Гіса та безперечному попередньому інфаркті міокарда, що маскує типові зміни.
б). Відсутність показань до тромболітичної терапії (пізні терміни, так званий дрібновогнищевий або не-Q-інфаркт), неможливість проведення тромболізису з організаційних причин, а також його відстрочення до госпітального етапу або деякі протипоказання до нього, які не є протипоказанням до призначення гепарину. при відсутності власних протипоказань до проведення антикоагулянтної терапії. Її мета полягає у попередженні або обмеженні тромбозу вінцевих артерій, а також у профілактиці тромбоемболічних ускладнень (особливо частих у хворих на передній інфаркт міокарда, при низькому серцевому викиді, миготливій аритмії). Для цього на догоспітальному етапі (лінійною бригадою) внутрішньовенно болюсно вводиться гепарин у дозі 10000-15000 МО. Якщо в умовах стаціонару не проводиться тромболітична терапія, то переходять на тривалу внутрішньовенну інфузію гепарину зі швидкістю 1000 МО/годину під контролем активованого часткового тромбопластинового часу. Альтернативою може, мабуть, служити підшкірне введення низькомолекулярного гепарину в лікувальній дозі. Введення гепарину на догоспітальному етапі не є перешкодою до проведення тромболізису в умовах стаціонару.
Незважаючи на більш високу безпеку гепаринотерапії порівняно із системним тромболізисом, у зв'язку із значно меншою її ефективністю ряд протипоказань до її проведення має значно жорсткіший характер, а деякі відносні протипоказання до тромболізису виявляються абсолютними для гепаринотерапії. З іншого боку, гепарин можна призначати хворим з деякими протипоказаннями до застосування тромполітичних засобів.
Для вирішення питання про можливість призначення гепарину слід уточнити ті самі моменти, що й для тромболитичних засобів:
- виключити наявність в анамнезі геморагічного інсульту, операцій на головному та спинному мозку;
- переконатися у відсутності пухлини та виразкової хворобишлунка та дванадцятипалої кишки, інфекційного ендокардиту, тяжкого ураження печінки та нирок;
- виключити підозру на гострий панкреатит, що розшаровує аневризму аорти, гострий перикардит із шумом тертя перикарда, що вислуховується протягом кількох днів (!) (Небезпека розвитку гемоперикарду);
- встановити відсутність фізикальних ознак або анамнестичних вказівок на патологію системи згортання крові (геморагічні діатези, хвороби крові);
З'ясувати, чи не має хворого підвищеної чутливості до гепарину;
- домогтися стабілізації підвищеного артеріального тиску лише на рівні менше 200/120 мм рт. ст.
У). З перших хвилин інфаркту міокарда всім хворим за відсутності протипоказань показано призначення малих доз ацетилсаліцилової кислоти (аспірину), антитромбоцитарний ефект якої досягає максимуму вже через 30 хвилин і своєчасне початок застосування якої дозволяє істотно знизити летальність. Найбільший клінічний ефект можна отримати при застосуванні ацетилсаліцилової кислотиперед проведенням тромболізису. Доза для першого прийому на догоспітальному етапі становить 160-325 мг розжувати (!). Надалі, на стаціонарному етапі препарат призначається 1 раз на добу по 100-125 мг.
Для вирішення питання про можливість призначення ацетилсаліцилової кислоти має значення лише невелика частина обмежень для тромболитичних засобів; необхідно уточнити:
Чи є у хворого ерозивно-виразкові ураження ШКТ у стадії загострення;
Чи були в анамнезі шлунково-кишкові кровотечі;
Чи немає у хворого на анемію;
- чи немає у хворого “аспіринової тріади” ( , поліпоз носа,
Непереносимість аспірину);
Чи є підвищена чутливість до препарату?
3. Зменшення роботи серця та потреби міокарда в кисні
крім повноцінного знеболювання забезпечується застосуванням
а) вазодилататорів - нітратів,
б) бета-адреноблокаторів та
в) засобами комплексного впливу – магнію сульфату.
А. Внутрішньовенне введення нітратівпри гострому інфаркті міокарда не тільки допомагає усунути больовий синдром, лівошлуночкову недостатність, артеріальну гіпертензію, а й зменшує розміри некрозу та летальність. Розчини нітратів для внутрішньовенного введення готують ex tempore: кожні 10 мг нітрогліцерину (наприклад, 10 мл 0,1 % розчину у вигляді перлінганіт) або ізосорбіду динітрату (наприклад, 10 мл 0,1 % розчину у вигляді препарату ізокет) розводять у 100 мл фізіологічного розчину(20 мг препарату – у 200 мл фізіологічного розчину тощо); таким чином, 1 мл приготовленого розчину містить 100 мкг, а 1 крапля - 5 мкг препарату. Нітрати вводять крапельно під постійним контролем артеріального тиску та частоти серцевих скорочень з початковою швидкістю 5-10 мкг/хв з подальшим збільшенням швидкості на 20 мкг/хв кожні 5 хвилин до досягнення бажаного ефекту або максимальної швидкості введення - 400 мкг/хв. Зазвичай ефект досягається при швидкості 50-100 мкг/хв. За відсутності дозатора приготовлений розчин, що містить в 1 мл 100 мкг нітрату, вводять при ретельному контролі (див. вище) з початковою швидкістю 6-8 крапель на хвилину, яка за умови стабільної гемодинаміки та збереження больового синдрому може бути поступово збільшена до максимальної швидкості - 30 крапель за хвилину. Введення нітратів проводиться як лінійними, і спеціалізованими бригадами і триває у стаціонарі. Тривалість внутрішньовенного введення нітратів – 24 години і більше; за 2-3 години до закінчення інфузії дається перша доза нітратів перорально. Передозування нітратів, що викликає падіння серцевого викиду та зниження систолічного артеріального тиску нижче 80 мм рт. ст., може призводити до погіршення коронарної перфузії та збільшення розмірів інфаркту міокарда.
Для вирішення питання щодо можливості призначення нітратів необхідно уточнити ряд моментів:
- переконатися, що систолічний артеріальний тиск вищий за 90 мм рт. ст. (Для короткодіючого нітрогліцерину) або вище 100 мм рт. ст (для більш тривалого діючого ізосорбіду динітрату);
- виключити наявність стенозу гирла аорти та гіпертрофічної кардіоміопатії з обструкцією виносного тракту (аускультативно і за даними ЕКГ), тампонаду серця (клінічна картина венозного застою по великому колу кровообігу при мінімальних ознаках лівошлуночкової недостатності) та констриктивний аперид "мале тихе серце");
- виключити внутрішньочерепну гіпертензію та гостру церебральну дисциркуляцію (у тому числі як прояви інсульту, гострої гіпертонічної енцефалопатії, нещодавно перенесеної черепно-мозкової травми);
- виключити можливість провокації нітратами розвитку синдрому малого викиду внаслідок ураження правого шлуночка при інфаркті або ішемії правого шлуночка, які можуть супроводжувати задню (нижню) локалізації інфаркту лівого шлуночка, або при тромбоемболії легеневої артерії з формуванням гострого легеневого серця;
- переконатися за допомогою пальпаторного обстеження без високого внутрішньоочного тиску (при закритокутовій глаукомі);
- уточнити, чи немає у хворого на непереносимість нітратів.
Б. Внутрішньовенне введення бета-адреноблокаторів
також як і застосування нітратів сприяє усуванню больового синдрому; послаблюючи симпатичні впливи на серце (ці впливи посилені в перші 48 годин інфаркту міокарда внаслідок самого захворювання та в результаті реакції на біль) та знижуючи потребу міокарда в кисні, вони сприяють зменшенню розмірів інфаркту міокарда, пригнічують шлуночкові аритмії, зменшують ризик розриву міокарда чином виживання пацієнтів. Дуже важливо, що бета-адреноблокатори згідно з експериментальними даними дозволяють відстрочити загибель ішемізованих кардіоміоцитів (вони збільшують час, протягом якого виявиться ефективним тромболізис).
За відсутності протипоказань бета-адреноблокатори призначаються всім хворим на гострий інфаркт міокарда. На догоспітальному етапі показаннями до їх внутрішньовенного введення служать для лінійної бригади - відповідні порушення ритму, а для спеціалізованої - наполегливий больовий синдром, тахікардія, артеріальна гіпертензія. У перші 2-4 години захворювання показано дробове внутрішньовенне введення пропранололу (обзидана) по 1 мг на хвилину кожні 3-5 хвилин під контролем артеріального тиску, частоти серцевих скорочень та ЕКГ до досягнення частоти серцевих скорочень 55-60 уд./хв або до загальної доза 10 мг. За наявності брадикардії, ознак серцевої недостатності, AV-блокакди та зниження систолічного артеріального тиску менше 100 мм рт. ст. пропранолол не призначається, а при розвитку зазначених змін на фоні його застосування препарат припиняється.
Для вирішення питання щодо можливості призначення бета-адреноблокаторів необхідно уточнити низку моментів:
- переконатися у відсутності гострої серцевої недостатності або недостатності кровообігу ІІ-ІІІ стадії, артеріальної гіпотензії;
- виключити наявність AV блокади, синоатріальної блокади, синдрому слабкості синусового вузла, брадикардії (ЧСС менше 55 ударів за хвилину);
- виключити наявність бронхіальної астмита інших обструктивних захворювань дихальних шляхів, а також вазомоторного риніту;
- виключити наявність облітеруючих захворювань судин (або ендартерит, синдром Рейно та ін.);
В) внутрішньовенна інфузія магнію сульфату
проводиться у хворих з доведеною або ймовірною гіпомагнезіємією або при подовженому синдромі QT, а також у разі ускладнення інфаркту міокарда деякими варіантами аритмій. За відсутності протипоказань магнію сульфат може бути певною альтернативою застосуванню нітратів і бета-адреноблокаторів, якщо їх введення з якоїсь причини неможливе (протипоказання або відсутність). За результатами низки досліджень він, як і інші засоби, що зменшують роботу серця та потребу міокарда в кисні, знижує летальність при гострому інфаркті міокарда, а також запобігає розвитку фатальних аритмій (у тому числі реперфузійних при проведенні системного тромболізису) та постінфарктної серцевої недостатності. При лікуванні гострого інфаркту міокарда 1000 мг магнію (50 мл 10 %, 25 мл 20 % або 20 мл 25 % розчину сірчанокислої магнезії) вводяться внутрішньовенно крапельно протягом 30 хвилин у 100 мл ізотонічного розчину натрію хлориду; надалі проводиться внутрішньовенна краплинна інфузія протягом доби зі швидкістю 100-120 мг магнію на годину (5-6 мл 10%, 2,5-3 мл 20% або 2-2,4 мл 25% розчину сірчанокислої магнезії).
Для вирішення питання про показання до призначення магнію сульфату необхідно уточнити ряд моментів:
- виявити клінічні та анамнестичні ознаки можливої гіпомагнезіємії – гіперальдостеронізм (насамперед при застійній серцевій недостатності та стабільній атреріальній гіпертензії), гіпертиреоз (у тому числі ятрогенний), хронічна алкогольна інтоксикація, судомні скорочення м'язів, тривале застосування діуретиків, глюкокортико;
- діагностувати наявність синдрому подовженого QT по ЕКГ
Для вирішення питання про можливість призначення магнію сульфату необхідно уточнити низку моментів:
- переконатися у відсутності станів, що виявляються гіпермагнезіємією - нирковою недостатністю, діабетичного кетоацидозу, гіпотиреоз;
- виключити наявність AV блокади, синоаурикулярної блокади, синдрому слабкості синусового вузла, брадикардії (ЧСС менше 55 ударів за хвилину);
Виключити наявність у хворого на міастенію;
- уточнити, чи немає у хворого на непереносимість препарату.
4. Обмеження розмірів інфаркту міокарда
досягається адекватним знеболенням, відновленням коронарного кровотоку та зменшенням роботи серця та потреби міокарда в кисні.
Цією ж метою служить оксигенотерапія, показана при гострому інфаркті міокарда всім хворим у зв'язку з частим розвитком гіпоксемії навіть при неускладненому перебігу захворювання. Інгаляція зволоженого кисню, що проводиться, якщо це не завдає надмірних незручностей, за допомогою маски або через носовий катетер зі швидкістю 4-6 л/хв, доцільна протягом перших 24-48 годин захворювання (починається на догоспітальному етапі і продовжується у стаціонарі).
5. Лікування та профілактика ускладнень інфаркту міокарда.
Усі перелічені заходи разом із забезпеченням фізичного та психічного спокою, госпіталізацією на ношах служать профілактиці ускладнень гострого інфаркту міокарда. Лікування ж у разі їх розвитку проводиться диференційовано залежно від варіанту ускладнень: набряк легень, кардіогенний шок, порушення серцевого ритму та провідності, а також тривалий або рецидивний больовий напад.
1). При гострій лівошлуночковій недостатності з розвитком серцевої астми або набряку легень одночасно з введенням наркотичних анальгетиків та нітрогліцерину внутрішньовенно струминно вводять 40-120 мг (4-12 мл) розчину фуросеміду (лазиксу), максимальна доза на догоспітальному етапі.
2). Основою лікування кардіогенного шоку служить обмеження зони ушкодження та збільшення обсягу функціонуючого міокарда шляхом покращення кровопостачання його ішемізованих ділянок, для чого проводиться системний тромболізис.
Аритмічний шок вимагає негайного відновлення адекватного ритму шляхом проведення електроімпульсної терапії, електрокардіостимуляції, при неможливості їх проведення показано медикаментозна терапія(Див. далі).
Рефлекторний шок купірується після проведення адекватної аналгезії; при вихідній брадикардії опіоїдні аналгетики слід поєднувати з атропіном у дозі 0,5 мг.
Справжній кардіогенний шок (гіпокінетичний тип гемодинаміки) служить свідченням до в/вкраплинного введення неглікозидних кардіотонічних (позитивних інотропних) засобів - допаміну, добутаміну, норепінефрину. Цьому має передувати корекція гіповолемії. За відсутності ознак застійної лівошлуночкової недостатності ОЦК коригується струминним введенням 0,9% розчину натрію хлориду в об'ємі до 200 мл за 10 хв повторним введеннямтієї ж дози за відсутності ефекту чи ускладнень.
Допамін у дозі 1-5 мкг/кг/хв має переважно вазодилатуючу дію, 5-15 мкг/кг/хв - вазодилатуючу та позитивну інотропну (і хронотропну) дію, 15-25 мкг/кг/хв. та периферичну вазоконстриктивну дію Початкова доза становить 2-5 мкг/кг/хв із поступовим збільшенням до оптимальної.
Добутамін на відміну від допаміну не викликає вазодилатацію, але має потужний позитивний інотропний ефект і менш виражене збільшення ЧСС та аритмогенний ефект. Препарат призначається в дозі 2,5 мкг/кг/хв зі збільшенням кожні 15-30 хв на 2,5 мкг/кг/хв до отримання ефекту, побічної діїабо досягнення дози 15 мкг/кг/хв.
Комбінація допаміну з добутаміном у максимально переносимих дозах використовується за відсутності ефекту від максимальної дозиодного з них або при неможливості використання максимальної дози одного препарату через побічні ефекти (синусова тахікардія більше 140 за хвилину або шлуночкова аритмія).
Комбінація допаміну або добутаміну з норепінефрином, що призначається у дозі 8 мкг/хв.
Норепінефрін (норадреналін) як монотерапія застосовується при неможливості використовувати інші пресорні аміни. Призначається в дозі, яка не перевищує 16 мкг/хв, в обов'язковому поєднанні з інфузією нітрогліцерину або ізосорбіду динітрату зі швидкістю 5-200 мкг/хв.
3). Шлуночкова екстрасистолія у гострій стадії інфаркту міокарда може бути провісником фібриляції шлуночків. Препарат вибору для лікування шлуночкових порушень ритму – лідокаїн – вводиться внутрішньовенно болюсом із розрахунку 1 мг/кг маси з подальшою крапельною інфузією 2-4 мг/хв. Не рекомендується профілактичне призначення лідокаїну, що застосовувалося раніше, всім хворим на гострий інфаркт міокарда (препарат збільшує летальність внаслідок асистолії). Хворим із застійною серцевою недостатністю, захворюваннями печінки, вводять у дозі, зниженій удвічі.
При шлуночковій тахікардії, тріпотінні передсердь та миготливої аритмії з високою ЧСС та нестабільною гемодинамікою засобом вибору є дефібриляція. При миготливій тахіаритмії та стабільній гемодинаміці використовують (анаприлін, обзидан) для ушкодження ЧСС.
При розвитку атріо-вентрикулярної блокади ІІ-ІІІ ступеня внутрішньовенно вводять 1 мл 0,1% розчину атропіну, при неефективності пробної терапії атропіном і появі непритомності (приступів Моргані-Едемса-Стокса) показана тимчасова електрокардіостимуляція.
ПОМИЛКИ ТЕРАПІЇ, що часто зустрічаються.
Висока летальність у перші години та добу інфаркту міокарда обумовлює необхідність призначення адекватної медикаментозної терапії, починаючи з перших хвилин захворювання. Втрата часу значно погіршує прогноз.
А. Помилки, зумовлені застарілими рекомендаціями, які частково зберігаються і в деяких сучасних стандартах надання медичної допомоги на догоспітальному етапі.
Найбільш поширеною помилкою є використання триступеневої схеми знеболювання: за відсутності ефекту від сублінгвального прийому нітрогліцерину перехід до наркотичних аналгетиків здійснюється лише після безуспішної спроби купувати больовий синдром за допомогою комбінації ненаркотичного анальгетика (метамізолу натрію – анальгіну) з антигістамінним препаратом. Тим часом, втрата часу при використанні такої комбінації, яка, по-перше, зазвичай не дозволяє отримати повноїаналгезії, а по-друге, не здатна на відміну від наркотичних аналгетиків забезпечити гемодинамічний розвантаження серця(головну мету знеболювання) та зменшити потребу міокарда в кисні, призводить до посилення стану та погіршення прогнозу.
Значно рідше, але все ще застосовуються міотропні спазмолітики (як виняток використовується папаверин, що рекомендувався раніше, на зміну якому прийшов дротаверин - но-шпа), що не покращують перфузію ураженої зони, але підвищують потребу міокарда в кисні.
Недоцільно застосування атропіну для профілактики (це не стосується купірування) вагоміметичних ефектів морфіну (нудота, блювання, вплив на серцевий ритмта артеріальний тиск), оскільки він може сприяти збільшенню роботи серця.
Профілактичне призначення лідокаїну, що рекомендується всім хворим на гострий інфаркт міокарда без урахування реальної ситуації, попереджаючи розвиток фібриляції шлуночків, може значно збільшувати летальність внаслідок настання асистолії.
Б. Помилки, зумовлені іншими причинами.
Дуже часто з метою знеболювання при ангінозному статусі невиправдано використовується комбінований препаратметамізол натрію з фенпіверином бромідом і пітофеноном гідрохлоридом (баралгін, спазмалгін, спазган і т. д.) або трамадол (трамал), що практично не впливають на роботу серця та споживання кисню міокардом, а тому не показані в цьому випадку (див. вище).
Вкрай небезпечно при інфаркті міокарда застосування як антиагрегантного засобу та “коронаролітика” дипірадомолу (курантила), що значно підвищує потребу міокарда в кисні.
Дуже поширеною помилкою є призначення калію і магнію аспартату (аспаркама, панангіна), що не впливає ні на зовнішню роботу серця, ні на споживання кисню міокардом, ні на коронарний кровотік і т.д.
ПОКАЗАННЯ ДО ГОСПІТАЛІЗАЦІЇ.
Гострий інфаркт міокарда є прямим показанням до госпіталізації у відділення (блок) інтенсивної терапії чи кардіореанімації. Транспортування здійснюється на ношах.

Загальні відомості
- Вогнище ішемічного некрозу серцевого м'яза, що розвивається в результаті гострого порушення коронарного кровообігу. Клінічно проявляється палючими, давящими або стискаючими болями за грудиною, що віддають у ліву руку, ключицю, лопатку, щелепу, задишкою, почуттям страху, холодним потом. Інфаркт міокарда, що розвинувся, служить показанням до екстреної госпіталізації в кардіологічну реанімацію. За ненадання своєчасної допомоги можливий летальний кінець.
У віці 40-60 років інфаркт міокарда в 3-5 разів частіше спостерігається у чоловіків у зв'язку з раннім (на 10 років раніше, ніж у жінок) розвитком атеросклерозу. Після 55-60 років захворюваність серед осіб обох статей приблизно однакова. Показник летальності при інфаркті міокарда становить 30-35%. Статистично 15-20% раптових смертей обумовлені інфарктом міокарда.
Порушення кровопостачання міокарда на 15-20 і більше хвилин призводить до розвитку незворотних змін у серцевому м'язі та розладу серцевої діяльності. Гостра ішемія викликає загибель частини функціональних м'язових клітин (некроз) та подальше їх заміщення волокнами сполучної тканини, Т. е. формування постінфарктного рубця.
У клінічному перебігуінфаркту міокарда виділяють п'ять періодів:
- 1 період– передінфарктний (продромальний): почастішання та посилення нападів стенокардії, може тривати кілька годин, доби, тижнів;
- 2 період– найгостріший: від розвитку ішемії до появи некрозу міокарда, що триває від 20 хвилин до 2 годин;
- 3 період– гострий: від утворення некрозу до міомаляції (ферментативного розплавлення некротизованої м'язової тканини), тривалість від 2 до 14 діб;
- 4 період- Підгострий: початкові процеси організації рубця, розвиток грануляційної тканини на місці некротичної, тривалість 4-8 тижнів;
- 5 період– постінфарктний: дозрівання рубця, адаптація міокарда до нових умов функціонування.

Причини інфаркту міокарда
Інфаркт міокарда є гострою формоюІХС. У 97-98% випадків основою для розвитку інфаркту міокарда служить атеросклеротична ураження вінцевих артерій, що викликає звуження їхнього просвіту. Нерідко до атеросклерозу артерій приєднується гострий тромбоз ураженої ділянки судини, що викликає повне або часткове припинення кровопостачання відповідної ділянки серцевого м'яза. Тромбоутворенню сприяє підвищена в'язкість крові, що спостерігається у пацієнтів з ІХС. У ряді випадків інфаркт міокарда виникає на тлі спазму гілок вінцевих артерій.
Розвитку інфаркту міокарда сприяють цукровий діабет, гіпертонічна хвороба, ожиріння, нервово-психічна напруга, захоплення алкоголем, куріння. Різка фізична або емоційна напруга на тлі ІХС та стенокардії може спровокувати розвиток інфаркту міокарда. Найчастіше розвивається інфаркт міокарда лівого шлуночка.
Класифікація інфаркту міокарда
Відповідно до розмірівосередкового ураження серцевого м'яза виділяють інфаркт міокарда:
- великовогнищевий
- дрібновогнищевий
На частку дрібноосередкових інфарктів міокарда припадає близько 20% клінічних випадків, проте нерідко дрібні осередки некрозу в серцевому м'язі можуть трансформуватися у великовогнищевий інфаркт міокарда (у 30% пацієнтів). На відміну від великовогнищевих, при дрібноочагових інфарктах не виникають аневризм і розрив серця, протягом останніх рідше ускладнюється серцевою недостатністю, фібриляцією шлуночків, тромбоемболією.
Залежно від глибини некротичної поразкисерцевого м'яза виділяють інфаркт міокарда:
- трансмуральний - з некрозом всієї товщі м'язової стінки серця (частіше великовогнищевий)
- інтрамуральний – з некрозом у товщі міокарда
- субендокардіальний – з некрозом міокарда у зоні прилягання до ендокарда
- субепікардіальний – з некрозом міокарда в зоні прилягання до епікарду
За змінами, що фіксуються на ЕКГ, Розрізняють:
- «Q-інфаркт» - з формуванням патологічного зубця Q, іноді шлуночкового комплексу QS (частіше великовогнищевий трансмуральний інфаркт міокарда)
- "не Q-інфаркт" - не супроводжується появою зубця Q, проявляється негативними Т-зубцями (частіше дрібноосередковий інфаркт міокарда)
По топографіїта залежно від ураження певних гілок коронарних артерій інфаркт міокарда поділяється на:
- правошлуночковий
- лівошлуночковий: передній, бічний і задній стінок, міжшлуночкової перегородки
За кратністю виникненнярозрізняють інфаркт міокарда:
- первинний
- рецидивуючий (розвивається у термін 8 тижнів після первинного)
- повторний (розвивається через 8 тижнів після попереднього)
З розвитку ускладненьінфаркт міокарда поділяється на:
- ускладнений
- неускладнений
За наявністю та локалізації больового синдромувиділяють форми інфаркту міокарда:
- типову – з локалізацією болю за грудиною або у прекардіальній ділянці
- атипові - з атиповими больовими проявами:
- периферичні: лівоопаточна, ліворукова, гортанно-глоточна, нижньощелепна, верхньохребетна, гастралгічна (черевна)
- безбольові: колаптоїдна, астматична, набрякла, аритмічна, церебральна
- малосимптомну (стерту)
- комбіновану
Відповідно до періоду та динамікирозвитку інфаркту міокарда виділяють:
- стадію ішемії (найгостріший період)
- стадію некрозу (гострий період)
- стадію організації (підгострий період)
- стадію рубцювання (постинфарктний період)
Симптоми інфаркту міокарда
Передінфарктний (продромальний) період
Близько 43% пацієнтів відзначають раптовий розвиток інфаркту міокарда, у більшості ж хворих спостерігається різний за тривалістю період нестабільної прогресуючої стенокардії.
Найгостріший період
Типові випадки інфаркту міокарда характеризуються надзвичайно інтенсивним больовим синдромом з локалізацією болів у грудній клітці та іррадіацією в ліве плече, шию, зуби, вухо, ключицю, нижню щелепу, міжлопаткову зону. Характер болю може бути стискаючим, розпираючим, пекучим, давящим, гострим («кинджальним»). Чим більше зонаураження міокарда, тим більше виражений біль.
Больовий напад протікає хвилеподібно (то посилюючись, то слабшаючи), триває від 30 хвилин до декількох годин, а іноді й доби, не усувається повторним прийомом нітрогліцерину. Біль пов'язаний із різкою слабкістю, збудженням, почуттям страху, задишкою.
Можливий атиповий перебіг найгострішого періоду інфаркту міокарда.
У пацієнтів відзначається різка блідість шкірних покривів, холодний липкий піт, акроціаноз, неспокій. Артеріальний тиску період нападу підвищено, потім помірно чи різко знижується проти вихідним (систолічне< 80 рт. ст., пульсовое < 30 мм мм рт. ст.), отмечается тахикардия , аритмия .
У цей період може розвинутись гостра лівошлуночкова недостатність (серцева астма, набряк легень).
Гострий період
У гострому періоді інфаркту міокарда больовий синдром, як правило, зникає. Збереження болів буває викликано вираженим ступенем ішемії при інфарктній зоні або приєднанням перикардиту.
Внаслідок процесів некрозу, міомаляції та перифокального запалення розвивається лихоманка (від 3-5 до 10 і більше днів). Тривалість та висота підйому температури при лихоманці залежать від площі некрозу. Артеріальна гіпотензія та ознаки серцевої недостатності зберігаються та наростають.
Підгострий період
Больові відчуття відсутні, стан пацієнта покращується, нормалізується температура тіла. Симптоми гострої серцевої недостатності стають менш вираженими. Зникає тахікардія, шум систоли.
Постінфарктний період
У постінфарктному періоді клінічні прояви відсутні, лабораторні та фізикальні дані практично без відхилень.
Атипові форми інфаркту міокарда
Іноді зустрічається атипова течія інфаркту міокарда з локалізацією болю в нетипових місцях (в області горла, пальцях лівої руки, в зоні лівої лопатки або шийно-грудного відділу хребта, в епігастрії, в нижній щелепі) або безболевих форм, ведучих важка ядуха, колапс, набряки, аритмії, запаморочення та потьмарення свідомості.
Атипові форми інфаркту міокарда частіше зустрічаються у пацієнтів похилого віку з вираженими ознаками кардіосклерозу, недостатністю кровообігу, на фоні повторного інфаркту міокарда.
Однак атипово протікає зазвичай лише найгостріший період, подальший розвитокІнфаркт міокарда стає типовим.
Стертий перебіг інфаркту міокарда буває безбольовим і випадково виявляється на ЕКГ.
Ускладнення інфаркту міокарда
Нерідко ускладнення виникають вже в перші години та дні інфаркту міокарда, обтяжуючи його перебіг. У більшості пацієнтів у перші три доби спостерігаються різні види аритмій: екстрасистолія, синусова або пароксизмальна тахікардія, миготлива аритмія, повна внутрішньошлуночкова блокада. Найбільш небезпечне мерехтіння шлуночків, яке може перейти у фібриляцію та призвести до загибелі пацієнта.
Лівошлуночкова серцева недостатність характеризується застійними хрипами, явищами серцевої астми, набряку легенів та нерідко розвивається у найгостріший період інфаркту міокарда. Вкрай важким ступенем лівошлуночкової недостатності є кардіогенний шок, що розвивається при обширному інфаркті і зазвичай призводить до летального результату. Ознаками кардіогенного шоку є падіння систолічного АТ нижче 80 мм рт. ст., порушення свідомості, тахікардія, ціаноз, зменшення діурезу.
Розрив м'язових волокон у зоні некрозу може викликати тампонаду серця – крововилив у порожнину перикарда. У 2-3% пацієнтів інфаркт міокарда ускладнюється тромбоемболіями системи легеневої артерії (можуть стати причиною інфаркту легень або раптової смерті) або великого колакровообігу.
Пацієнти з великим трансмуральним інфарктом міокарда у перші 10 діб можуть загинути від розриву шлуночка внаслідок гострого припинення кровообігу. При великому інфаркті міокарда може виникати неспроможність рубцевої тканини, її вибухання з недостатнім розвитком гострої аневризми серця. Гостра аневризм може трансформуватися в хронічну, що призводить до серцевої недостатності.
Відкладення фібрину на стінках ендокарда призводить до розвитку пристінкового тромбоендокардиту, небезпечного можливістю емболії судин легень, мозку, нирок тромботичними масами, що відірвалися. У пізнішому періоді може розвинутись постінфарктний синдром, що проявляється перикардитом, плевритом, артралгіями, еозинофілією.
Діагностика інфаркту міокарда
Серед діагностичних критеріїв інфаркту міокарда найважливішими є анамнез захворювання, характерні зміни на ЕКГ, показники активності ферментів сироватки. Скарги пацієнта при інфаркті міокарда залежать від форми (типової або атипової) захворювання та обширності ураження серцевого м'яза. Інфаркт міокарда слід запідозрити при тяжкому та тривалому (довше 30-60 хвилин) нападі загрудинних болів, порушенні провідності та ритму серця, гострій серцевій недостатності.
До характерних змін ЕКГ належать формування негативного зубця Т (при дрібноочаговому субендокардіальному або інтрамуральному інфаркті міокарда), патологічного комплексу QRS або зубця Q (при великовогнищевому трансмуральному інфаркті міокарда). При ЕхоКГ виявляється порушення локально скоротливості шлуночка, стоншення його стінки.
У перші 4-6 годин після больового нападу в крові визначається підвищення міоглобіну - білка, що здійснює транспорт кисню всередину клітин. через дві доби. Визначення рівня КФК проводять через кожних 6-8 годин. Інфаркт міокарда виключається за трьох негативних результатів.
Для діагностики інфаркту міокарда на пізніших термінах вдаються до визначення ферменту лактатдегідрогенази (ЛДГ), активність якої підвищується пізніше КФК – через 1-2 доби після формування некрозу і приходить до нормальних значень через 7-14 днів. Високоспецифічним для інфаркту міокарда є підвищення ізоформ міокардіального скорочувального білка тропоніну - тропоніну-Т і тропоніну-1, що збільшуються також при нестабільної стенокардії. У крові визначається збільшення ШОЕ, лейкоцитів, активності аспартатамінотрансферази (АсАт) та аланінамінотрансферази (АлАт).
Коронарна ангіографія (коронарографія) дозволяє встановити тромботичну оклюзію коронарної артерії та зниження шлуночкової скоротливості, а також оцінити можливості проведення аортокоронарного шунтування чи ангіопластики – операцій, що сприяють відновленню кровотоку в серці.
Лікування інфаркту міокарда
При інфаркті міокарда показана екстрена госпіталізація до кардіологічної реанімації. У гострому періоді пацієнту наказується постільний режим та психічний спокій, дробове, обмежене за обсягом та калорійністю харчування. У підгострому періоді хворий переводиться з реанімації у відділення кардіології, де триває лікування інфаркту міокарда та здійснюється поступове розширення режиму.
Купірування больового синдрому проводиться поєднанням наркотичних аналгетиків (фентанілу) з нейролептиками (дроперидолом), внутрішньовенним введенням нітрогліцерину.
Терапія при інфаркті міокарда спрямована на запобігання та усунення аритмій, серцевої недостатності, кардіогенного шоку. Призначають антиаритмічні засоби (лідокаїн), β-адреноблокатори (атенолол), тромболітики (гепарин, ацетилсаліцилова кислота), антогоністи Са (верапаміл), магнезію, нітрати, спазмолітики тощо.
У перші 24 години після розвитку інфаркту міокарда можна провести відновлення перфузії шляхом тромболізису або екстреної балонної коронарної ангіопластики.
Прогноз при інфаркті міокарда
Інфаркт міокарда є важким, пов'язаним із небезпечними ускладненнями захворюванням. Більшість летальних наслідків розвивається першу добу після інфаркту міокарда. Насосна здатність серця пов'язана з локалізацією та обсягом зони інфаркту. При пошкодженні понад 50% міокарда, як правило, серце функціонувати не може, що спричиняє кардіогенний шок та загибель пацієнта. Навіть при меншому пошкодженні серце не завжди справляється навантаженнями, внаслідок чого розвивається серцева недостатність.
Після закінчення гострого періоду прогноз на одужання непоганий. Несприятливі перспективи у пацієнтів із ускладненим перебігом інфаркту міокарда.
Профілактика інфаркту міокарда
Необхідними умовами профілактики інфаркту міокарда є ведення здорового та активного способу життя, відмова від алкоголю та куріння, збалансоване харчування, виключення фізичного та нервового перенапруги, контроль АТ та рівня холестерину крові.